题目内容
(2010?溧阳市模拟)有A、B、C、D、E五种常见物质,它们有如下图所示关系: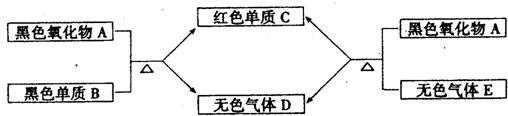
已知:C是一种金属,气体D可以使澄清石灰水变浑浊.
(1)写出物质的名称:A
(2)写出A和B、A和E反应的化学方程式

已知:C是一种金属,气体D可以使澄清石灰水变浑浊.
(1)写出物质的名称:A
氧化铜
氧化铜
、C铜
铜
、D二氧化碳
二氧化碳
、E、一氧化碳
一氧化碳
(2)写出A和B、A和E反应的化学方程式
C+2CuO
2Cu+CO2↑;
| ||
C+2CuO
2Cu+CO2↑;
、
| ||
CO+CuO
Cu+CO2
| ||
CO+CuO
Cu+CO2
.
| ||
分析:根据物质转化关系图及物质说明,可判断红色金属单质C为金属单质铜,可以使澄清石灰水变浑浊的气体D为二氧化碳;以此作为推断的突破口,根据物质间的反应关系、转化关系,对其它四种物质进行推断,利用推断结果完成问题的解答.
解答:解:(1)根据红色金属单质C为铜、可以使澄清石灰水变浑浊的无色气体D为二氧化碳,由物质转化关系图可判断,黑色氧化物为氧化铜、黑色单质B为木炭粉、无色气体E应为具有还原性的气体一氧化碳;
故答案为:氧化铜;铜;二氧化碳,一氧化碳;
(2)黑色氧化物A为氧化铜与黑色单质B木炭粉发生置换反应,木炭粉在高温条件下夺取氧化铜中的氧变成二氧化碳,氧化铜失去氧变成红色金属单质铜;一氧化碳与氧化铜反应生成铜和二氧化碳.
故答案为:C+2CuO
2Cu+CO2↑;CO+CuO
Cu+CO2
故答案为:氧化铜;铜;二氧化碳,一氧化碳;
(2)黑色氧化物A为氧化铜与黑色单质B木炭粉发生置换反应,木炭粉在高温条件下夺取氧化铜中的氧变成二氧化碳,氧化铜失去氧变成红色金属单质铜;一氧化碳与氧化铜反应生成铜和二氧化碳.
故答案为:C+2CuO
| ||
| ||
点评:利用物质的典型特点确定物质,使得推断有个突破口,完成物质的推断;利用推断结果完成转化过程中的问题.

练习册系列答案
相关题目