题目内容
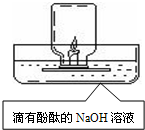 16、如图所示,某同学设计了测定空气中氧气的体积分数的实验.实验结束时量得进入集气瓶中水的体积小于集气瓶容积的1/5.以下分析不正确的是( )
16、如图所示,某同学设计了测定空气中氧气的体积分数的实验.实验结束时量得进入集气瓶中水的体积小于集气瓶容积的1/5.以下分析不正确的是( )分析:根据空气中氧气含量的测定的原理,要求生成物是固体,而蜡烛燃烧却是能够生成二氧化碳甚至还可能生成一氧化碳,所以实验者设计了用氢氧化钠来吸收二氧化碳的这个细节,所以酚酞的加入虽然开始可以便于观察液面的变化,但是最终目的是证明二氧化碳被吸收.而对于进入液体小于 $\frac{1}{5}$,我们有时会考虑药品的量不足,但是本题中蜡烛熄灭了,说明蜡烛是有剩余的.所以分析时就要注意到这一点.
解答:解:
A、在起始阶段确实便于液面变化的观察,但是后期红色消失,所以便于观察一说不成立,加入的本意是通过颜色变化证明二氧化碳被反应掉,从而引起液面上升.错误.
B、开始由于水中有氢氧化钠,所以先红色.后来随着反应的进行,二氧化碳进入溶液从而消耗了溶液中的氢氧化钠,使红色消失.正确.
C、进入集气瓶中水的体积偏少可能是因为瓶内的氧气没有完全消耗.由于燃烧需要氧气达到一定的浓度,所以后期蜡烛熄灭并不代表氧气被完全消耗,所以会导致进入液体体积偏小.正确.
D、其实用蜡烛或者木炭都不可能得到对应的结果,因为这个过程中随着氧气浓度的降低,过程中会生成一氧化碳,虽然可以用氢氧化钠来吸收二氧化碳,但是一氧化碳却无法被吸收.正确.
故答案:A
A、在起始阶段确实便于液面变化的观察,但是后期红色消失,所以便于观察一说不成立,加入的本意是通过颜色变化证明二氧化碳被反应掉,从而引起液面上升.错误.
B、开始由于水中有氢氧化钠,所以先红色.后来随着反应的进行,二氧化碳进入溶液从而消耗了溶液中的氢氧化钠,使红色消失.正确.
C、进入集气瓶中水的体积偏少可能是因为瓶内的氧气没有完全消耗.由于燃烧需要氧气达到一定的浓度,所以后期蜡烛熄灭并不代表氧气被完全消耗,所以会导致进入液体体积偏小.正确.
D、其实用蜡烛或者木炭都不可能得到对应的结果,因为这个过程中随着氧气浓度的降低,过程中会生成一氧化碳,虽然可以用氢氧化钠来吸收二氧化碳,但是一氧化碳却无法被吸收.正确.
故答案:A
点评:实验设计中要对各种情况考虑周全,比如蜡烛一般考虑生成二氧化碳,但是却忽略生成一氧化碳.

练习册系列答案
相关题目
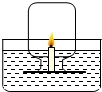 如图所示,某同学设计了测定空气中氧气的体积分数的实验.在水槽中盛适量的稀氢氧化钠溶液,并滴入2~3滴酚酞试液,在小木片上固定一只短蜡烛(普通蜡烛1cm,或者生日蜡烛2~3cm),用火柴点燃蜡烛.把集气瓶倒扣在小木块上方,并将瓶口水封.几秒钟后,蜡烛火焰熄灭,水位上升.在水下用玻片盖上集气瓶,取出,量得集气瓶中水的体积小于集气瓶容积的
如图所示,某同学设计了测定空气中氧气的体积分数的实验.在水槽中盛适量的稀氢氧化钠溶液,并滴入2~3滴酚酞试液,在小木片上固定一只短蜡烛(普通蜡烛1cm,或者生日蜡烛2~3cm),用火柴点燃蜡烛.把集气瓶倒扣在小木块上方,并将瓶口水封.几秒钟后,蜡烛火焰熄灭,水位上升.在水下用玻片盖上集气瓶,取出,量得集气瓶中水的体积小于集气瓶容积的| 1 |
| 5 |
| A、滴入2~3滴酚酞试液的目的是让溶液变红,便于观察集气瓶中的水位上升 |
| B、滴入酚酞试液后,一开始溶液变红,随着蜡烛的燃烧,溶液逐渐褪色 |
| C、进入集气瓶中水的体积偏少可能是因为瓶内的氧气没有完全消耗 |
| D、进入集气瓶中水的体积偏少可能是因为随着瓶内的氧气减少,蜡烛发生了不完全燃烧,生成了不能被氢氧化钠溶液吸收的CO等气体 |
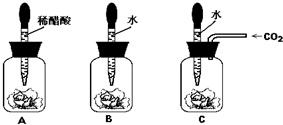
 如图所示为某同学设计的制取氧气的实验装置图
如图所示为某同学设计的制取氧气的实验装置图