题目内容
【题目】A、B、 C、D、E、F、G、H分别是硝酸银溶液、碳酸钠溶液、稀盐酸、氢氧化钙溶液、硫酸铜溶液、铁丝、氧化铁和水八种物质中的一种;用连线表示物质能反应,用箭头表示物质可以转化。试回答下列问题: (不考虑氢氧化银)
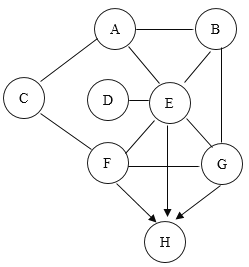
(1)在圆内写出各物质(或溶质)的化学式________。
(2) E与D反应的化学方程式:__________________。
(3)B与G反应的实验现象:__________________。
【答案】A.Fe,B.AgNO3,C.CuSO4,D.Fe2O3,E.HCl,F.Ca(OH)2,G.Na2CO3,H.H2O Fe2O3+6HCl═2FeCl3+3H2O 白色沉淀生成
【解析】
A、B、 C、D、E、F、G、H分别是硝酸银溶液、碳酸钠溶液、稀盐酸、氢氧化钙溶液、硫酸铜溶液、铁丝、氧化铁和水八种物质中的一种, E能与A、B、D、F、G五种物质反应,其中盐酸刚能与硝酸银、碳酸钠、氢氧化钙、铁和氧化铁五种物质反应,所以E是稀盐酸,且氧化铁只能与盐酸反应,所以D是氧化铁;又E、F、G都能转化生成H,盐酸和碱反应生成水、碳酸钠和酸反应有水生成、氢氧化钙和酸反应也有水生成,所以H是水,如果F是氢氧化钙,则G是碳酸钠;G碳酸钠能与B反应;A、B分别是是铁、硝酸银中的一种,因为硝酸银能与G碳酸钠反应生成碳酸银沉淀,所以B是硝酸银,A是铁;最后剩余的硫酸铜是C,经验证,推到正确。
(1)A是Fe,B是AgNO3,C是CuSO4,D是Fe2O3,E是HCl,F是Ca(OH)2,G是Na2CO3,H是H2O。
故填:A.Fe,B.AgNO3,C.CuSO4,D.Fe2O3,E.HCl,F.Ca(OH)2,G.Na2CO3,H.H2O。
(2)E与D反应是稀盐酸和氧化铁反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O。
故填:Fe2O3+6HCl═2FeCl3+3H2O。
(3)B与G反应是硝酸银和碳酸钠反应生成碳酸银沉淀和硝酸钠,现象是有白色沉淀生成。
故填:白色沉淀生成。

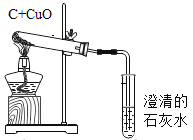
【题目】实验课上,同学们利用澄清石灰水检验空气中的二氧化碳,实验中发现各组石灰水浑浊程度存在较大差异,于是设计实验探究影响石灰水浑浊程度的因素。
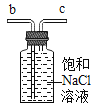
(进行实验)装置图如下所示。

实验1:取饱和澄清石灰水进行实验。
实验序号 | 1-1 | 1-2 | 1-3 | 1-4 |
饱和澄清石灰水体积/mL | 2.0 | 1.5 | 1.0 | 0.5 |
缓慢通入2 L空气后的浑浊程度 | 不明显 | 明显 | 非常明显 | 明显 |
实验2:利用向饱和石灰水中添加蒸馏水来调节石灰水浓度进行实验(溶液浓度变化引起的溶液密度变化忽略不计)。
实验序号 | 2-1 | 2-2 | 2-3 | 2-4 |
饱和澄清石灰水体积/mL | 2.0 | 1.5 | 1.0 | 0.5 |
加入蒸馏水体积/mL | 0 | a | b | c |
缓慢通入3 L空气后的浑浊程度 | 非常明显 | 明显 | 不明显 | 无现象 |
(解释与结论)
(1)小试管中发生反应的化学方程式为____________。
(2)实验1的目的为____________。
(3)实验2中a、b、c三处数据,设计合理的是________。
A 0.5 0.5 0.5 B 0.5 1.0 1.5
C 1.0 1.5 2.0 D 1.0 2.0 3.0
(4)实验2的结论是________。
(反思与评价)
(5)通过对比实验1-1和2-1,可得出影响石灰水浑浊程度的另一因素是________,理由是________。