题目内容
【题目】某化学兴趣小组的同学发现:许多无明显现象的化学反应,可通过滴加其他试剂的方法使之产生明显的现象,以证明反应的发生。他们做了以下三个实验。
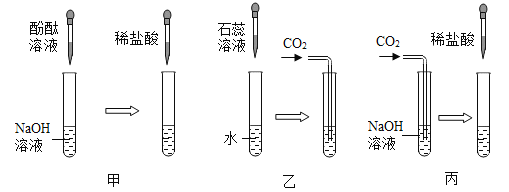
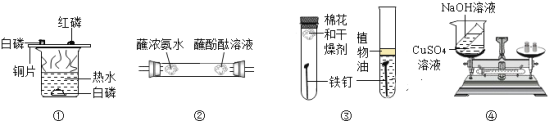
[现象分析](1)甲实验中表明NaOH溶液与稀盐酸发生了反应的现象是_______。
(2)乙实验中观察到石蕊溶液由紫色变为红色,说明CO2能与水反应生成____ (填“酸性”、“碱性”或“中性”)物质。
(3)丙实验滴入稀盐酸后。观察到溶液中有气泡冒出,写出产生气泡的化学方程式__,此现象说明CO2与NaOH溶液能发生反应。同学们经过讨论,一致认为通入CO2后的溶液中滴入______________溶液,观察到有白色沉淀生成,也可以得出相同结论。
[交流讨论]由上述实验得知,实验乙是通过检验有新物质生成证明反应发生,与乙采用了相同原理的还有实验___ (填“甲”或“丙”)。
[归纳结论]对于无明显现象的化学实验,既可以通过检验有新物质生成证明反应的发生,也可以通过证明_____来证明反应的发生。
[拓展迁移]小明查阅资料获知,氢氧化钠与酒精不发生化学反应,但能溶于酒精形成无色透明溶液,氢氧化钠的酒精溶液与氢氧化钠的水溶液化学性质相似,碳酸钠不与酒精反应也不溶于酒精。根据上述信息,请你帮助小明完成下列实验。
实验操作 | 实验现象 | 实验结论 |
(1)取一定量的氢氧化钠固体于烧杯中,向其中加入适量的酒精溶液。 (2)向上述溶液中通入二氧化碳气体 | ___ | NaOH与CO2能发生化学反应。 |
【答案】溶液由红色变成无色 酸性 ![]() 氯化钙(合理即可) 丙 反应物的消失 有白色沉淀产生
氯化钙(合理即可) 丙 反应物的消失 有白色沉淀产生
【解析】
{现象分析}
(1)氢氧化钠溶液呈碱性,向氢氧化钠溶液中加入酚酞溶液后溶液变红,再加入稀盐酸,当氢氧化钠完全与盐酸反应后,溶液不再呈碱性,观察到溶液由红色变成无色。
(2)酸性溶液能够使紫色石蕊溶液变红,将二氧化碳通入到滴有石蕊溶液的水中,观察到紫色石蕊溶液变红,说明二氧化碳与水反应后的物质的溶液呈酸性,故填酸性。
(3)二氧化碳能与氢氧化钠反应生成碳酸钠和水,加入的稀盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,观察到产生气泡,故反应的化学方程式写为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
加入稀盐酸产生气泡,说明溶液中含有碳酸钠,证明碳酸钠存在,除用盐酸证明外,还可以向溶液中滴加含有钙离子的溶液,如氯化钙溶液等于碳酸钠反应生成白色沉淀来证明碳酸钠存在,故填氯化钙等。
{交流讨论}
丙实验通过滴加盐酸产生气泡来证明溶液中含有碳酸根离子,说明溶液中含有碳酸钠,进而证明二氧化碳与氢氧化钠发生了反应,故填丙。
{归纳结论}
对于无明显现象的化学实验,既可以通过检验有新物质生成证明反应的发生,也可以通过证明反应物的消失来证明反应的发生,如甲实验中通过酚酞溶液颜色的变化来证明氢氧化钠消失说明氢氧化钠与盐酸发生了反应,故填反应物消失。
{拓展迁移}
氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠不溶于酒精,所以实验中观察到的现象是液体中有白色沉淀产生,故填有白色沉淀产生。

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】某学校科学兴趣小组设计一个实验,来模拟研究CO2浓度增加是否导致地球温室效应增强。他们的实验和操作步骤如下:
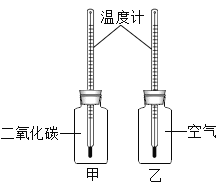
Ⅰ.在两只相同的玻璃瓶里分别充满CO2和空气,并编号为甲、乙,塞紧带有同样温度计的橡皮塞。再把两只玻璃瓶放在阳光下照射(如上图所示),观察甲、乙瓶中的温度变化。
Ⅱ.阳光持续照射,间隔一定时间测量两只玻璃瓶温度值,并记录在下表中:
时间 | 9︰23 | 9︰28 | 9︰33 | 9︰38 | 9︰43 | 9︰48 | 9︰53 | 9︰58 | 10︰06 | 10︰11 | 10︰25 |
甲瓶温度/C | 13.0 | 19.8 | 23.5 | 26.0 | 26.4 | 27.0 | 27.5 | 27.8 | 28.0 | 28.0 | 28.1 |
乙瓶温度/ C | 13.0 | 19.0 | 22.8 | 25.0 | 26.0 | 26.5 | 27.0 | 27.4 | 27.9 | 28.0 | 28.1 |
请完成下列空白:
(1)往瓶中充CO2时,验证瓶中已充满了CO2的方法是_________________________________。
(2)该实验中,照射同样时间,根据上表的数据,比较甲、乙瓶温度变化的规律是__________。
(3)有同学认为根据该模拟实验的目的,实验设计存在问题,你认为有什么问题?(写出一点即可) _________________________________。
【题目】2020年1月25日总建筑面积为3.39万平方米的火神山医院正式开工,火神山医院在建造过程中用到了HDPE膜. HDPE膜具有极好的抗冲击性和防潮性,某探究小组对HDPE膜的组成元素进行了如下探究。
[提出问题] HDPE膜由什么元素组成?
[查阅资料]①HDPE膜能够燃烧,燃烧可能生成一氧化碳;
②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
[实验探究]如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D (装置中每步反应均进行完全)。
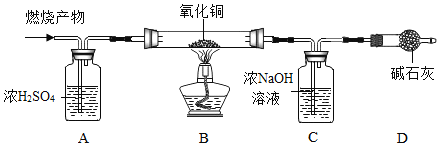
[实验记录]
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2g |
[实验分析]
(1)装置A中浓硫酸的作用是________。
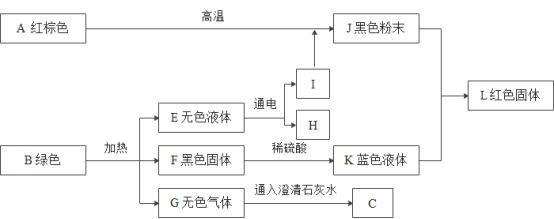
(2)实验中观察到装置B中黑色粉末变成红色,证明燃烧产物中有________。
(3)装置B中发生的化学反应方程式为_________。
(4)分析反应后装置C中的溶质。取适量C中溶液于烧杯中,加入______溶液, 静置,再滴加____;产生白色沉淀,溶液变红色;则溶液中含有的溶质是_____。
[实验结论]
(5)HDPE膜由元素_____(填元素符号)组成。
(6)某工厂每天要烧掉含硫1.6%的烟煤100吨,排放出的SO2严重地污染环境。如果用石灰乳吸收这些二氧化硫,至少需要熟石灰________吨。