题目内容
 以下是我省生产的某种钙盐包装标签上的部分文字.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.请计算此加钙食盐中钙元素的质量分数. .
以下是我省生产的某种钙盐包装标签上的部分文字.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.请计算此加钙食盐中钙元素的质量分数. .
【答案】分析:欲正确解答本题,需写出碳酸钙与盐酸反应的化学方程式,得出各物质之间的质量比,列出比例式,就可计算出样品中CaCO3的质量,然后根据碳酸钙的化学式计算出CaCO3中Ca的质量分数,进而计算出样品中钙的质量,再根据质量分数公式计算即可.
解答:解:设参加反应CaCO3的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 0.132g
∴
解之得:x=0.3g,
CaCO3中Ca的质量分数为: =40%,
=40%,
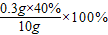 =1.2%.
=1.2%.
故答案为:1.2%.
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力.
解答:解:设参加反应CaCO3的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 0.132g
∴

解之得:x=0.3g,
CaCO3中Ca的质量分数为:
 =40%,
=40%,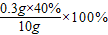 =1.2%.
=1.2%.故答案为:1.2%.
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目

 以下是我省生产的某种钙盐包装标签上的部分文字.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.请计算此加钙食盐中钙元素的质量分数.
以下是我省生产的某种钙盐包装标签上的部分文字.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.请计算此加钙食盐中钙元素的质量分数.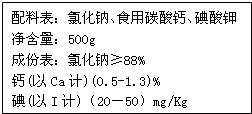
 以下是我省生产的某种加钙食盐包装袋上的部分文字,请仔细阅读以后
以下是我省生产的某种加钙食盐包装袋上的部分文字,请仔细阅读以后 以下是我省生产的某种加钙食盐包装袋上的部分文字,请仔细阅读以后
以下是我省生产的某种加钙食盐包装袋上的部分文字,请仔细阅读以后