题目内容
北京奥运会将进行火炬登珠峰活动.2005年5月22日,中国登山测量队成功登上珠峰峰顶,圆满完成珠峰高度最新测量工作.登山队员常用的能源是氢化钙(CaH2)固体,用它和水反应生成氢氧化钙和氢气
[CaH2+2H2O=Ca(OH)2+2H2↑],氢气供燃烧之需.请回答下列问题:
(1)CaH2中钙元素为+2价,氢元素的化合价为________.
(2)现有875g氢化钙固体(含CaH296%),与足量水反应可生成多少克氢气?
解:(1)设氢化钙中氢元素的化合价为x.
(+2)+x×2=0
x=-1;
(2)生成氢气的质量为y.
CaH2+2H2O=Ca(OH)2+2H2↑
42 4
875g×96% y
 =
=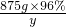 ,y=80g
,y=80g
答:(1)-1价.
(2)可生成80g氢气.
分析:(1)化合物中元素的化合价的代数和为零.
化合物中金属元素一般显正价,非金属元素一般显负价.
化合物中钙元素常显+2价.
(2)由氢化钙的质量和质量分数根据氢化钙与水反应的化学方程式可以计算出生成氢气的质量.
点评:本题主要考查有关化学式的计算和含杂质物质的化学方程式计算,难度较大.
(+2)+x×2=0
x=-1;
(2)生成氢气的质量为y.
CaH2+2H2O=Ca(OH)2+2H2↑
42 4
875g×96% y
 =
=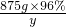 ,y=80g
,y=80g答:(1)-1价.
(2)可生成80g氢气.
分析:(1)化合物中元素的化合价的代数和为零.
化合物中金属元素一般显正价,非金属元素一般显负价.
化合物中钙元素常显+2价.
(2)由氢化钙的质量和质量分数根据氢化钙与水反应的化学方程式可以计算出生成氢气的质量.
点评:本题主要考查有关化学式的计算和含杂质物质的化学方程式计算,难度较大.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目