题目内容
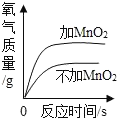
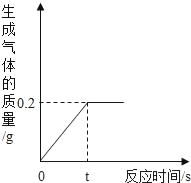
【题目】 化学兴趣小组的同学取10g铜锌合金样品于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7g时,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题:
(1)样品中锌的质量为_____ g。
(2)反应后,所得溶液中溶质的质量分数为多少________?
【答案】6.5 16.1%
【解析】
由图中数据可知生成氢气的质量,根据氢气的质量可以计算锌和生成硫酸锌的质量,进一步可以计算溶液中硫酸锌的质量分数。
(1)由图可知完全反应后生成氢气的质量为0.2g,
设锌的质量为x,生成硫酸锌的质量为y
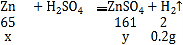
![]() ;解得:x=6.5g y=16.1g;故填:6.5
;解得:x=6.5g y=16.1g;故填:6.5
(2)反应后所得溶液中溶质的质量分数为:![]()
答:反应后,所得溶液中溶质的质量分数为16.1%。故填:16.1%

【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____________。
【查阅资料】CaC12 滚液显中性
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想I:只有CaC12 猜想II:有__________
猜想III:有CaC12和Ca(OH)2 猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是_________________。
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ____________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
【得出结论】通过探究,全班同学一致确定猜想III是正确的。
【评价反思】(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____________。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑_______。
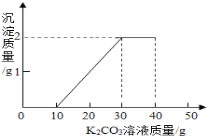
【题目】某公司生产的新型融雪剂的成分是无水CaCl2和少量的氯化钠,为测定融雪剂中氯化钙的含量,化学兴趣小组的同学称取该样品12g,加水充分溶解,得到溶液50g,然后取一定质量分数的碳酸钠溶液100g平均分五次加入,充分振荡,实验数据见表。请你分析数据并进行有关计算。
次 数 | 1 | 2 | 3 | 4 | 5 |
加入碳酸钠溶液的质量/g | 20 | 20 | 20 | 20 | 20 |
生成沉淀的质量/g | 2.5 | x | 7.5 | 10 | 10 |
(1)上表中x的数值为_____。第_____次加入的碳酸钠与氯化钙恰好完全反应。
(2)样品中氯化钙的质量分数是多少_____?
(3)恰好完全反应时过滤,所得不饱和溶液的溶质质量分数是多少_____?
【题目】已知A、B、C三种物质有如图转化关系(→箭头表示反应一步实现,部分物质和反应条件已略去)则符合A、B、C是( )
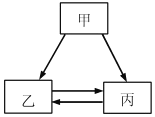
选项 | 甲 | 乙 | 丙 |
A | H2SO4 | H2 | H2O |
B | C | CO | CO2 |
C | Ca(OH)2 | CaCl2 | CaCO3 |
D | NaOH | NaCl | NaNO3 |
A. AB. BC. CD. D
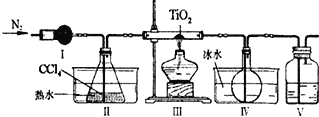
【题目】某小组以固态TiO2和气态CCl4为原料在无氧、无水的条件下制取液态TiCl4,反应的化学方程式是:TiO2(固态)+CCl4(气态)═TiCl4(气态)+CO2(气态),实验装置和相关数据如下(熔点和沸点为101.3千帕时测得)。下列分析错误的是
物质 | 熔点 | 沸点 | 其他性质 |
CO2 | -78℃ | -78℃ | 不易溶于CCl4 |
CCl4 | -23℃ | 76℃ | 与TiCl4互溶 |
TiCl4 | -25℃ | 136℃ | 遇潮湿空气产生白雾 |
A. 实验过程中应持续通入氮气
B. 热水的温度不低于76℃
C. 冰水使生成物全部液化
D. 装置V中的试剂为浓硫酸,其作用是防止空气中的水和氧气进入装置