题目内容
利用家庭生活用品可以对化学知识进行学习和探究.食盐、食醋、纯碱均为家庭厨房中常用的物质,利用这些物质能完成的实验为
A、检验自来水中是否含有氯离子 B、除去热水瓶中的水垢
C、鉴别BaCl2溶液和CaCl2溶液 D、 .
A、检验自来水中是否含有氯离子 B、除去热水瓶中的水垢
C、鉴别BaCl2溶液和CaCl2溶液 D、
考点:化学实验方案设计与评价,证明盐酸和可溶性盐酸盐,盐的化学性质
专题:简单实验方案的设计与评价
分析:A、根据氯离子的检验方法分析即可;
B、根据水垢的主要成分是碳酸钙及碳酸钙的性质分析即可;
C、根据钡离子的检验方法分析即可;
D、根据鸡蛋壳的主要成分是碳酸钙及碳酸钙与酸的反应原理分析即可.
B、根据水垢的主要成分是碳酸钙及碳酸钙的性质分析即可;
C、根据钡离子的检验方法分析即可;
D、根据鸡蛋壳的主要成分是碳酸钙及碳酸钙与酸的反应原理分析即可.
解答:解:A、实验室用硝酸酸化的硝酸银溶液检验氯离子,厨房中没有硝酸和硝酸银溶液,故A错误;
B、水垢的主要成分是碳酸钙,而食醋中含醋酸,碳酸钙可以与醋酸反应,所以可用食醋除去热水瓶中的水垢,故B正确;
C、实验室用硝酸酸化的硫酸盐溶液检验钡离子,厨房中没有硝酸和硫酸盐溶液,故C错误;
D、鸡蛋壳的主要成分是碳酸钙,醋酸可以与碳酸钙反应,所以可以用食醋检验鸡蛋壳能否溶于酸.
故答案为:B;检验鸡蛋壳能否溶于酸.
B、水垢的主要成分是碳酸钙,而食醋中含醋酸,碳酸钙可以与醋酸反应,所以可用食醋除去热水瓶中的水垢,故B正确;
C、实验室用硝酸酸化的硫酸盐溶液检验钡离子,厨房中没有硝酸和硫酸盐溶液,故C错误;
D、鸡蛋壳的主要成分是碳酸钙,醋酸可以与碳酸钙反应,所以可以用食醋检验鸡蛋壳能否溶于酸.
故答案为:B;检验鸡蛋壳能否溶于酸.
点评:要清楚常见物质的主要成分,如食醋中含醋酸,鸡蛋壳的主要成分是碳酸钙,纯碱是碳酸钠,另外要熟练掌握常见离子的检验.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列化学方程式中,正确的是( )
| A、CuO+H2O═Cu(OH)2 |
| B、Mg(OH)2+2HCl═MgCl2+2H2O |
| C、Zn(NO3)2+2KCl═ZnCl2+2KNO3 |
| D、Cu+ZnSO4═CuSO4+Zn |
2013年4月5日,国家食品药品监督管理总局批准了抗流感新药帕拉米韦氯化钠注射液,现有临床试验数据证明其对新发的H7N9人禽流感患者具有显著的治疗作用.下列有关帕拉米韦(C15H28N4O4)的说法不正确的是( )
| A、由C、H、N、O四种元素组成 |
| B、一个分子中含2个氧分子 |
| C、相对分子质量328 |
| D、属于有机化合物 |
小薇自制了几支“吹不灭的蜡烛”,点燃后即使用力吹灭火焰,蜡烛也会很快复燃,这种蜡烛之所以具有熄而复燃的特点,是因为在烛芯中加入了某种金属粉末X,将X粉末放入少量盐酸中有大量气泡产生,待反应停止后,向反应后溶液中加入锌粒,无明显现象,则X、Zn、Cu三种金属活动性由强到弱的顺序是( )
| A、Zn、X、Cu |
| B、X、Zn、Cu |
| C、Zn、Cu、X |
| D、Cu、X、Zn |
 近期,媒体报道的食品安全问题--染色瓜子,成为公众的焦点.绿茶瓜子跟茶叶完全“不沾边”、工业滑石粉让瓜子外表光鲜亮丽…日前,上视新闻曝光炒货市场乱象,绿茶瓜子实际上是使用色素亮蓝(化学式为C37H34N2Na2O9S3)浸泡而成,另据报道,为了使瓜子光滑且色泽明亮,不少炒货厂商还违规添加工业滑石粉,明矾[化学式KAI(SO4)2?12H2O]、焦亚硫酸钠(化学式为Na2S2O5)等对人体有害的物质也在炒货的制作过程中超量使用.试回答下列问题:
近期,媒体报道的食品安全问题--染色瓜子,成为公众的焦点.绿茶瓜子跟茶叶完全“不沾边”、工业滑石粉让瓜子外表光鲜亮丽…日前,上视新闻曝光炒货市场乱象,绿茶瓜子实际上是使用色素亮蓝(化学式为C37H34N2Na2O9S3)浸泡而成,另据报道,为了使瓜子光滑且色泽明亮,不少炒货厂商还违规添加工业滑石粉,明矾[化学式KAI(SO4)2?12H2O]、焦亚硫酸钠(化学式为Na2S2O5)等对人体有害的物质也在炒货的制作过程中超量使用.试回答下列问题: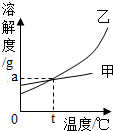 图示为甲和乙两种固体物质的溶解度曲线.根据该图可知甲物质的溶解度受温度影响变化不大.此外你还能获得的信息有:
图示为甲和乙两种固体物质的溶解度曲线.根据该图可知甲物质的溶解度受温度影响变化不大.此外你还能获得的信息有: