题目内容
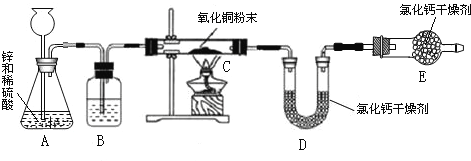
【题目】(4分)某同学用氢气还原灼热氧化铜的方法测定水的组成(装置如下图所示)
请回答:
(1)B装置中盛放的液体是_______,作用是_.
(2)C装置中观察到的现象是________________________________.
(3)E装置的作用是_______________________.如果不连接E装置,得出的实验结论中氢氧元素的质量比_______________(填大于、小于或等于)理论值.
【答案】(1)浓硫酸,吸收氢气中的水分.(2)黑色粉末逐渐变成红色块状固体.(3)防止空气中的水进入D装置.大于
【解析】
试题分析:(1)锌和稀硫酸反应产生的氢气中含有水分,与氧化铜反应的氢气必须是干燥的,则B中盛放的是浓硫酸,浓硫酸具有吸水性;(2)黑色粉末逐渐变成光亮的红色固体;(3)E装置的作用是吸收空气中的水分,防止空气中的水分进入D装置,使最终测得水的质量偏大,从而导致水中氢氧元素的质量比大于理论值。

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目