题目内容
某密闭容器中有W、氧气、二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,根据表中信息,判断下列说法正确的是( )
A.待测数值为6g
B.W一定不是氧化物
C.CO2是反应物,H2O是生成物
D.反应中CO2和H2O质量变化之比为23:18
| 物质 | W | O2 | CO2 | H2O |
| 反应前质量/g | 16 | 72 | 2 | 0 |
| 反应后质量/g | 0 | 待测 | 46 | 36 |
A.待测数值为6g
B.W一定不是氧化物
C.CO2是反应物,H2O是生成物
D.反应中CO2和H2O质量变化之比为23:18
B
试题分析:A、根据质量守恒定律可以知道,“待测”=16+72+2+0﹣0﹣46﹣36=8,故说法错误;B、根据反应前后质量的变化可以判断二氧化碳和水为生成物,而W和氧气为反应物,根据反应前后元素的种类不变可以知道,在W中含有碳元素和氢元素,又参加反应的44g二氧化碳中碳元素的质量44g×(
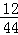 ×100%)=12g,参加反应的36g水中氢元素的质量36g×(
×100%)=12g,参加反应的36g水中氢元素的质量36g×(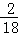 ×100%)=4g,12g+4g=16g,和参加反应的W的质量相等,因此W中只含有碳、氢两种元素,一定不是氧化物,故说法正确;C、根据二氧化碳和水的质量反应后增加可知两者都是生成物,故说法错误;D、反应中生成二氧化碳的质量为:46g﹣2g=44g,生成水的质量为36g,其质量比为44g:36g=22:18,故说法错误
×100%)=4g,12g+4g=16g,和参加反应的W的质量相等,因此W中只含有碳、氢两种元素,一定不是氧化物,故说法正确;C、根据二氧化碳和水的质量反应后增加可知两者都是生成物,故说法错误;D、反应中生成二氧化碳的质量为:46g﹣2g=44g,生成水的质量为36g,其质量比为44g:36g=22:18,故说法错误
练习册系列答案
相关题目
 CO+H2
CO+H2


