题目内容
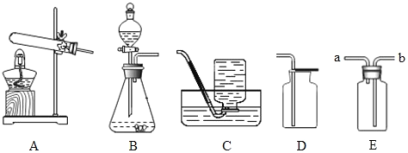
【题目】探究空气中氧气含量的实验(如图所示),回答下列问题:
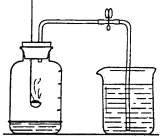
(1)甲同学点燃燃烧匙中的红磷,观察到红磷燃烧,放热,并产生大量的_________,该反应的文字表达式___________。冷却后,打开弹簧夹,出现___________的现象。
(2)乙同学用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏小,其原因可能是__________________。(要求答出一种)
(3)实验结束后,集气瓶中剩余的气体主要是氮气,且瓶内水面上升到一定高度后不再上升了,由此分析说明,氮气具有的一条性质:________________________________。
(4)丙同学探究能否用镁条代替红磷,将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁的粉末。请写出镁在氮气中燃烧反应的文字表达式________________,分析后认为________(填“能”或“不能”)代替红磷,原因是_____________。若用镁代替红磷实验,进入瓶中水的体积会________(填 > 或< 或 =)瓶内空气体积的1/5.
(5)下列有关测定空气中氧气含量实验说法正确的是___________(填字母).
A.燃烧匙中的红磷越多,水位上升越高
B.本实验可以证明空气含有N2、O2、CO2和稀有气体.
C.选用红磷是因为只能与空气中的氧气反应,且生成物为固体
D.集气瓶中先装入少量水是为了吸收生成物,防止污染空气
【答案】白烟磷+氧气![]() 五氧化二磷烧杯中的水沿导管进入集气瓶,进入瓶中水的体积约占瓶内空气体积的1/5。红磷的量不足氮气难溶于水镁+氮气
五氧化二磷烧杯中的水沿导管进入集气瓶,进入瓶中水的体积约占瓶内空气体积的1/5。红磷的量不足氮气难溶于水镁+氮气![]() 氮化镁不能镁能与空气中的氮气反应 。〉CD
氮化镁不能镁能与空气中的氮气反应 。〉CD
【解析】
(1)红磷燃烧放出热量,产生大量的白烟;红磷燃烧的文字表达式为磷+氧气![]() 五氧化二磷;待温度冷却后打开止水夹,可以看到的现象是烧杯中的水沿导管进入集气瓶,进入瓶中水的体积约占瓶内空气体积的1/5;
五氧化二磷;待温度冷却后打开止水夹,可以看到的现象是烧杯中的水沿导管进入集气瓶,进入瓶中水的体积约占瓶内空气体积的1/5;
(2)该实验的成功要注意三个关键点:一是气密性良好,二是红磷过量,三是带温度冷却后才能打开止水夹,否则会使测量结果偏小;
(3)实验室结束后有氮气剩余,说明氮气不支持燃烧,也不溶于水;
(4)镁与氮气在点燃的条件下反应生成氮化镁,文字表达式为镁+氮气![]() 氮化镁;不能用镁来代替红磷进行该实验,因为镁不仅可以与氧气反应,而且可以与氮气反应,故会使测量结果偏大;故进入瓶中的水的体积会大于瓶内空气体积的1/5;
氮化镁;不能用镁来代替红磷进行该实验,因为镁不仅可以与氧气反应,而且可以与氮气反应,故会使测量结果偏大;故进入瓶中的水的体积会大于瓶内空气体积的1/5;
(5)A、该实验中要求红磷要过量,目的是为了耗尽瓶中的氧气,当瓶中的氧气耗尽后,再过量的红磷就没有用处了,故水位上升到一定的高度后不再上升,故错误;
B、本实验只能证明空气中含有氧气和不与红磷反应的物质,不能证明剩余气体是氮气、二氧化碳等,故错误;
C、红磷只能与空气中的氧气反应,不能与其他气体反应,且生成的物质是固体五氧化二磷,不影响空气中氧气的测定,故正确;
D、该实验中集气瓶中加入少量的水,目的是吸收生成的五氧化二磷固体和热量,防止该物质逸散到空气中污染空气,故正确。故选CD。

 阅读快车系列答案
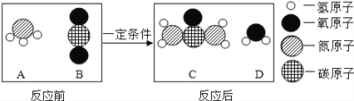
阅读快车系列答案【题目】如图表示某化学反应的微观过程,下列说法正确的是( )
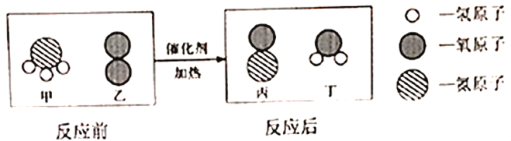
A. 该反应属于置换反应
B. 甲物质由一个氮原子和三个氢原子构成
C. 生成丙和丁的分子个数比为2:3
D. 化学反应前后,元素的种类发生了变化
【题目】实验小组的同学将CO2通入氢氧化钠溶液时,没有观察到明显现象。为了能通过实验现象证明二氧化碳与氢氧化钠确实发生了反应,进行了以下探究。
(提出问题)如何能观察到反应的变化过程?
(查阅资料)
NaOH、Na2CO3在水中的溶解度
温度/℃ | 0 | 10 | 20 | 30 |
NaOH | 42 | 51 | 109 | 119 |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaOH、Na2CO3在乙醇中的溶解度
温度/℃ | NaOH | Na2CO3 |
18.5~25 | 17.3 | 不溶 |
(进行实验)注:乙醇在实验中只作为溶剂,不参与化学反应。
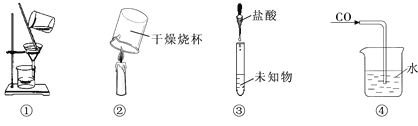
实验 | 实验装置 | 实验操作 | 实验现象 |
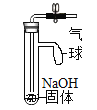
1 |
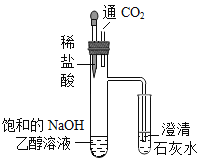
| 打开止水夹,通入 CO2,气球明显鼓起后关闭止水夹 | 一段时间后,气球明显变瘪 |
2/p> |
| 室温下,向10mL澄清饱和的NaOH溶液中通入适量CO2 | 试管内壁出现白色固体 |
3 |
| ① 室温下,向10mL饱和的NaOH乙醇溶液中缓慢通入适量CO2 | 甲中出现白色沉淀,乙中无明显现象 |
② 滴入稀盐酸 | 甲中有气泡生成,乙中澄清石灰水变浑浊 |
(解释与结论)
(1)二氧化碳与氢氧化钠反应的化学方程式为_______。
(2)实验1中,气球明显变瘪的原因是_______。
(3)实验2中,试管内壁上出现白色固体的原因是_______。
(4)实验3甲中出现白色沉淀的原因是_______。
(5)实验3中操作②的目的是_______。
(反思与评价)
(6)实验1是从________(填“反应物消耗”或“新物质生成”)角度证明化学反应发生。
【题目】暖贴发热是利用了铁粉生锈放出热量的原理,某小组同学设计并进行实验,探究铁生锈的条件及影响生锈速率的因素。
I.探究铁生锈的条件
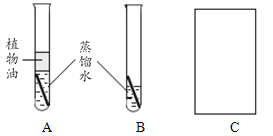
(1)由实验B和C得出铁生锈需要与水接触,画出实验C的实验装置图。__________
(2)证明铁生锈需要与氧气接触的实验现象是____________。
II.探究影响铁生锈速率的因素
(查阅资料)暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
(猜想假设)
(1)活性炭能加快铁粉生锈的速率。
(2)食盐能加快铁粉生锈的速率。
(进行实验)下表是2g铁粉、5g水与不同量活性炭、食盐均匀混合后,在10分钟内温度上升的实验记录。
实验编号 | 活性炭/g | 食盐/g | 温度上升值/℃ |
1 | 0 | 0 | 0.1 |
2 | 0.2 | 0 | 22.0 |
3 | x | 0.1 | 3.1 |
4 | 0.2 | 0.1 | 56.3 |
(解释与结论)
(3)表中x的值为____________。
(4)对比实验1和3,得出的结论是____________。
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁生锈速率”,需要对比________(填实验编号)。
(反思与评价)
(6)下列说法正确的是_______。
A.暖贴在使用前要密封保存
B.暖贴使用后剩余物可以回收利用
C.利用铁生锈的原理,铁粉还可用于食品保鲜