题目内容
聚乳酸[(C3H4O2)n]是一种对人体无毒无害且可生物降解的理想的高分子环保材料,合成聚乳酸的材料是乳酸,1个乳酸分子中含有3个碳原子.在乳酸完全燃烧生成水和二氧化碳的实验中,有9g乳酸与一定质量的O2反应生成了13.2gCO2和5.4g H2O.
(1)通过计算确定乳酸的化学式.
(2)完成该反应的化学方程式:
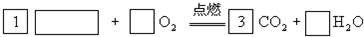
解:(1)13.2gCO2中C元素的质量=13.2g×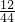 ×100%=3.6g;5.4g H2O中H元素的质量=5.4g×
×100%=3.6g;5.4g H2O中H元素的质量=5.4g×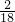 ×100%=0.6g;
×100%=0.6g;
根据质量守恒定律可知乳酸中O元素质量为9g-3.6g-0.6g=4.8g;
则乳酸中C、H、O原子个数比为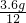 :
: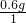 :
: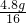 =1:2:1,据题意“1个乳酸分子中含有3个碳原子”得出:
=1:2:1,据题意“1个乳酸分子中含有3个碳原子”得出:
乳酸的化学式为:C3H6O3.
答:乳酸的化学式为C3H6O3.
(2)乳酸在O2中完全燃烧生成CO2和H2O,其燃烧的化学方程式为C3H6O3+3O2 3CO2+3H2O;
3CO2+3H2O;
故答案为:C3H6O3;3;3.
分析:根据乳酸完全燃烧,其中C元素全部生成二氧化碳、H元素全部生成水;由生成的13.2gCO2和5.4g H2O分别计算出有机物中C、H元素质量和,然后计算出乳酸中氧元素的质量,由有机物中C、H、O元素的质量及有相对原子质量推断乳酸的化学式,然后完成燃烧的化学方程式.
点评:本题难度不大,掌握有关化学式的计算以及化学方程式的书写方法是解题的关键.
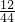 ×100%=3.6g;5.4g H2O中H元素的质量=5.4g×
×100%=3.6g;5.4g H2O中H元素的质量=5.4g×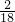 ×100%=0.6g;
×100%=0.6g;根据质量守恒定律可知乳酸中O元素质量为9g-3.6g-0.6g=4.8g;
则乳酸中C、H、O原子个数比为
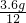 :
: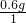 :
: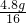 =1:2:1,据题意“1个乳酸分子中含有3个碳原子”得出:
=1:2:1,据题意“1个乳酸分子中含有3个碳原子”得出:乳酸的化学式为:C3H6O3.
答:乳酸的化学式为C3H6O3.
(2)乳酸在O2中完全燃烧生成CO2和H2O,其燃烧的化学方程式为C3H6O3+3O2
 3CO2+3H2O;
3CO2+3H2O;故答案为:C3H6O3;3;3.
分析:根据乳酸完全燃烧,其中C元素全部生成二氧化碳、H元素全部生成水;由生成的13.2gCO2和5.4g H2O分别计算出有机物中C、H元素质量和,然后计算出乳酸中氧元素的质量,由有机物中C、H、O元素的质量及有相对原子质量推断乳酸的化学式,然后完成燃烧的化学方程式.
点评:本题难度不大,掌握有关化学式的计算以及化学方程式的书写方法是解题的关键.

练习册系列答案
相关题目