题目内容
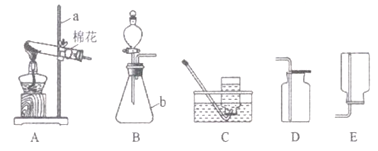
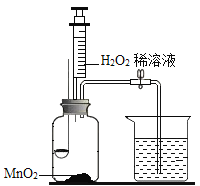
【题目】某同学用如图所示装置.分别进行“燃烧条件”和“氧气性质”的探究实验(已知:白磷的着火点为40℃)。请回答下列问题:
内容步骤 | (实验1)燃烧条件 | (实验2)氧气性质 |
1 | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞; | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞; |
2 | 推入H2O2溶液 | 推入H2O2溶液 |
(1)H2O2与MnO2接触时,发生反应的化学方程式为___________________,MnO2起_________作用。
(2)实验1中,推入H2O2溶液,燃烧匙和水中的白磷均不燃烧,原因分别是___、____;打开止水夹,推入H2O2溶液,观察到烧杯中的现象是_______。
(3)实验2中打开止水夹,推入H2O2溶液,观察到木炭燃烧得更剧烈,由此得出氧气的性质是_______,木炭熄灭冷却一段时间后,烧杯中的部分溶液流入集气瓶,该实验开始时到实验结束后,集气瓶内压强的变化过程是___________。
【答案】2H2O2![]() 2H2O+ O2↑ 催化 温度未达到白磷的着火点 没有与氧气接触 烧杯中的白磷燃烧 具有助燃性 先增大后减小
2H2O+ O2↑ 催化 温度未达到白磷的着火点 没有与氧气接触 烧杯中的白磷燃烧 具有助燃性 先增大后减小
【解析】
(1)过氧化氢在二氧化锰的催化作用下生成水和氧气;故填:2H2O2![]() 2H2O+ O2↑;催化;
2H2O+ O2↑;催化;
(2)根据燃烧的条件可知,燃烧匙中白磷不燃烧是因为未达到白磷的着火点,烧杯中白磷未燃烧是因为没有与O2接触;推入H2O2溶液后,生成氧气,氧气通过导管进入烧杯,所以观察到烧杯中的现象是导管口有气泡冒出,因为热水的温度达到了白磷的着火点,所以热水中的白磷燃烧;故填:燃烧匙中白磷不燃烧是因为未达到白磷的着火点;烧杯中白磷未燃烧是因为没有与O2接触;导管口有气泡冒出,白磷燃烧;
(3)实验2中打开止水夹,推入H2O2溶液,过氧化氢在二氧化锰的催化作用下生成了氧气,观察到木炭燃烧得更剧烈,由此得出氧气具有助燃性;该实验开始是木炭燃烧放热,所以集气瓶内压强增大,反应后生成的二氧化碳被氢氧化钠吸收所以集气瓶内压强又减小,溶液倒吸入集气瓶内,所以最后恢复至常压。故填:具有助燃性;先增大后减小。

 华东师大版一课一练系列答案
华东师大版一课一练系列答案【题目】下列图像表述的化学事实与实际相符的是
A | B | C | D | |
图象 |
|
|
|
|
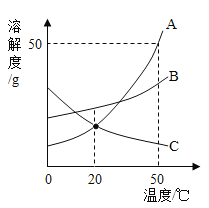
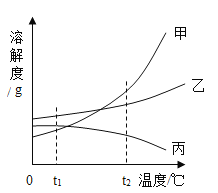
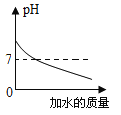
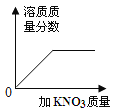
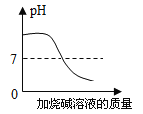
实验或事实 | 向pH=12的Ca(OH)2溶液中不断加水稀释 | 20C时,向一杯不饱和的KNO3溶液中逐步加入KNO3晶体 | 向稀盐酸中滴加过量的烧碱溶液 | 将一定质量的MnO2和KClO混合加热 |
A. AB. BC. CD. D