题目内容
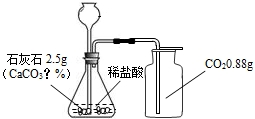
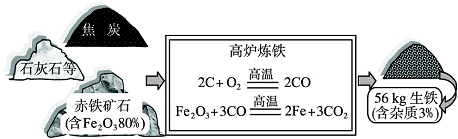
请你利用下图中所提供的信息,自拟一道有关化学方程式的计算题,并写出解答过程.
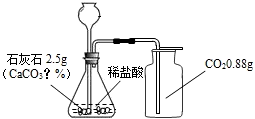
解:取样品石灰石2.5克,向其加入足量的稀盐酸,生成了0.88克的二氧化碳.则石灰石的纯度是多少?
设碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 0.88g
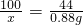 ,x=2g
,x=2g
石灰石的纯度=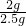 ×100%=80%
×100%=80%
答:石灰石的纯度是80%.
分析:根据题意找出已知量和未知量,已知量是石灰石2.5g,和盐酸反应生成二氧化碳0.88g,未知量是石灰石样品的纯度,然后加上适当的文字说明即可.
解答为:根据二氧化碳的质量求出碳酸钙的质量,再根据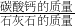 ×100%求出石灰石样品的纯度.
×100%求出石灰石样品的纯度.
点评:本题比较灵活,要先根据所给信息自拟一道有关化学方程式的计算题,然后进行解答,解题关键是根据图示找出已 知量和未知量,然后加入相应的文字说明即可.
设碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 0.88g
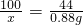 ,x=2g
,x=2g石灰石的纯度=
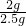 ×100%=80%
×100%=80% 答:石灰石的纯度是80%.
分析:根据题意找出已知量和未知量,已知量是石灰石2.5g,和盐酸反应生成二氧化碳0.88g,未知量是石灰石样品的纯度,然后加上适当的文字说明即可.
解答为:根据二氧化碳的质量求出碳酸钙的质量,再根据
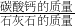 ×100%求出石灰石样品的纯度.
×100%求出石灰石样品的纯度.点评:本题比较灵活,要先根据所给信息自拟一道有关化学方程式的计算题,然后进行解答,解题关键是根据图示找出已 知量和未知量,然后加入相应的文字说明即可.

练习册系列答案
相关题目
请你利用下图中所提供的3个数据,自拟一道有关化学方程式的计算题,并写出解答过程。
| 自拟试题内容部分 | 自拟试题解答部分 |