题目内容
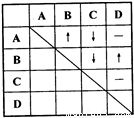
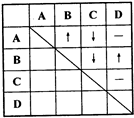 25、为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成).
25、为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成).(1)四种物质的化学式分别是:
A
H2SO4
BNa2CO3
CBa(OH)2
DHCl
(2)写出有关反应的离子方程式:
A+B:
2H++CO32-═H2O+CO2↑
C+D:H++OH-═H2O
A+C:
2H++SO42-+2OH-+Ba2+═2H2O+BaSO4↓
B+C:Ba2++CO32-═BaCO3↓
.分析:分析所给的四种物质之间能发生反应的为:氢氧化钡可以和碳酸钠及稀硫酸反应生成沉淀,碳酸钠能和稀硫酸、盐酸、硝酸钡反应,盐酸可以和碳酸钠反应生成气体,稀硫酸可以和氢氧化钡和碳酸钠反应,可以据此来解答该题.
解答:解:(1)从表格中的反应可知:A和B反应生成气体,B和D反应有气体逸出,故可以判断B为碳酸钠,而A和D分别为盐酸和稀硫酸,那么C为氢氧化钡;根据A和C生成沉淀,D和C反应没有现象可知:A为硫酸,D为盐酸.
(2)根据(1)中的解答可以知道A和B的反应为硫酸和碳酸钠的反应,C和D的反应为氢氧化钡和盐酸的反应,A和C反应为硫酸和氢氧化钡反应,B和C反应为碳酸钠与氢氧化钡反应,有关反应的离子方程式为:
A+B:2H++CO32-═H2O+CO2↑; C+D:H++OH-═H2O;
A+C:2H++SO42-+2OH-+Ba2+═2H2O+BaSO4↓ B+C:Ba2++CO32-═BaCO3↓.
故答案为:(1)H2SO4;Na2CO3;Ba(OH)2;HCl;
(2)A+B:2H++CO32-═H2O+CO2↑; C+D:H++OH-═H2O;
A+C:2H++SO42-+2OH-+Ba2+═2H2O+BaSO4↓ B+C:Ba2++CO32-═BaCO3↓.
(2)根据(1)中的解答可以知道A和B的反应为硫酸和碳酸钠的反应,C和D的反应为氢氧化钡和盐酸的反应,A和C反应为硫酸和氢氧化钡反应,B和C反应为碳酸钠与氢氧化钡反应,有关反应的离子方程式为:
A+B:2H++CO32-═H2O+CO2↑; C+D:H++OH-═H2O;
A+C:2H++SO42-+2OH-+Ba2+═2H2O+BaSO4↓ B+C:Ba2++CO32-═BaCO3↓.
故答案为:(1)H2SO4;Na2CO3;Ba(OH)2;HCl;
(2)A+B:2H++CO32-═H2O+CO2↑; C+D:H++OH-═H2O;
A+C:2H++SO42-+2OH-+Ba2+═2H2O+BaSO4↓ B+C:Ba2++CO32-═BaCO3↓.
点评:此类问题一般采取:利用物质间相互反应所出现实验现象与探究实验所观察到的现象进行对比,完成对物质进行推断.

练习册系列答案
相关题目
 (2012?宜昌)在“课内比教学”活动中,老师和化学兴趣小组的同学一起对初中化学常见物质进行了如下探究.
(2012?宜昌)在“课内比教学”活动中,老师和化学兴趣小组的同学一起对初中化学常见物质进行了如下探究.



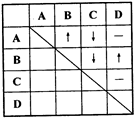 为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成).
为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成).