题目内容
 小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:
小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:第一组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装人其总容积10%、20%、30%、40%、50%的水.用排水法收集氧气,恰好把5只集气瓶中的水排去.将带火星的木条依次插入①~⑤号瓶中,记录实验现象.
小亮在前一组实验的基础上又做了第二组和第三组实验,三组实验的数据和现象见表.
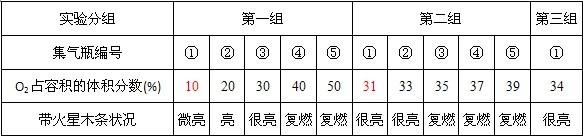
| 实验分组 | 第一组 | 第二组 | 第三组 | ||||||||
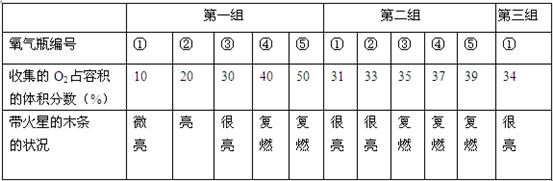
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| O2占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 | 34 |
| 带火星木条状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
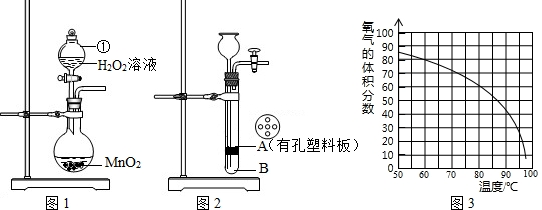
(1)写出实验室用高锰酸钾制取氧气的文字表达式
高锰酸钾
锰酸钾+二氧化锰+氧气
| △ |
高锰酸钾
锰酸钾+二氧化锰+氧气
.| △ |
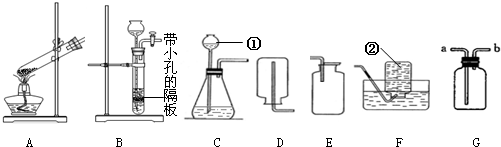
(2)在使用双氧水和二氧化锰制取的装置中,使用分液漏斗的优点是
控制反应的发生
控制反应的发生
,此反应中二氧化锰起催化
催化
作用;(3)使用带火星的木条验满氧气的方法是否可靠:
否
否
(填“是”或“否’').(4)集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数×
21
21
%.(5)收集的氧气占容积的体积分数最低为
35
35
%时,可使带火星的木条复燃,这时集气瓶中氧气分数是49
49
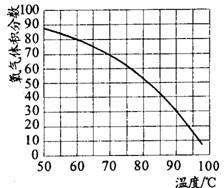
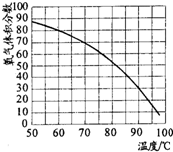
%(计算结果保留整数).(6)用带火星的木条直接检验双氧水受热分解产生的氧气时,往往难以复燃,这是因为在加热生成氧气的同时产生大量水蒸汽所致,此时混合气体中氧气的体积分数随温度变化的曲线如图所示.若只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,应将加热双氧水的最高温度控制在
82
82
℃.(7)采取“半值法”探究能减少实验次数.例如:第一组实验若按③、④的编号顺序进行实验,即可确定下一组实验收集的氧气占容积的体积分数应在30%~40%之间,从而省去编号为①、②、⑤的实验.同理,第二组实验可以省去的实验编号为
①、④、⑤
①、④、⑤
.分析:本题通过实验探究了能使带火星的木条复燃的氧气含量的最低值问题,针对此问题,设计了几组氧气含量不同的对照实验.通过实验可以看出,不是纯净的氧气,带火星的木条也可以复燃;分析表格可发现收集的氧气占容积的体积分数最低为35%时木条就可复燃,根据空气中原有的氧气和收集到的氧气,就可算出氧气的分数;“半值法”的应用可以减少实验的次数,节约时间,确定时采用的一般是中间值.
解答:解:(1)高锰酸钾在加热的情况下,生成了二氧化锰、锰酸钾和氧气,其表达式为高锰酸钾
锰酸钾+二氧化锰+氧气;
(2)分液漏斗能够控制双氧水的滴加从而控制反应的发生;在双氧水制氧气的过程中二氧化锰所起的作用是催化作用.
(2)检验装置的气密性时,通常将活塞关闭,将导管伸入到水中,然后用双手握住锥形瓶,观察水中是否有气泡产生.
(3)通过实验可以看出,氧气含量达到35%带火星的木条就可以复燃,所以用带火星的木条验满氧气的方法不可靠;
(4)由题干所提供的条件可知:集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数×空气中氧气的体积分数.
(5)由图中可知,当氧气的体积分数达到35%时,带火星的木条复燃.此时空气还占65%,所以空气中有氧气的量为:65%×21%≈14%,所以此时瓶内共有氧气的分数为:14%+35%=49%;
(6)只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,则氧气的含量需要在48%~49%,分析坐标,可知道温度大约在82℃左右;
(7)采取“半值法”探究能减少实验次数,实际上就是通过实验数据的分析,减少不必要的实验,第二组实验若按②、③的编号顺序进行实验,即可确定下一组实验收集的氧气占容积的体积分数应在33%~35%之间,从而省去编号①、④、⑤的实验.
故答案为:(1)、高锰酸钾→锰酸钾+二氧化锰+氧气;
(2)、分液漏斗能够控制反应的发生;催化;
(3)、否;
(4)、21%;
(5)、35%; 49%(计算结果保留整数);
(6)、82;
(7)、①、④、⑤.
| △ |
(2)分液漏斗能够控制双氧水的滴加从而控制反应的发生;在双氧水制氧气的过程中二氧化锰所起的作用是催化作用.
(2)检验装置的气密性时,通常将活塞关闭,将导管伸入到水中,然后用双手握住锥形瓶,观察水中是否有气泡产生.
(3)通过实验可以看出,氧气含量达到35%带火星的木条就可以复燃,所以用带火星的木条验满氧气的方法不可靠;
(4)由题干所提供的条件可知:集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数×空气中氧气的体积分数.
(5)由图中可知,当氧气的体积分数达到35%时,带火星的木条复燃.此时空气还占65%,所以空气中有氧气的量为:65%×21%≈14%,所以此时瓶内共有氧气的分数为:14%+35%=49%;
(6)只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,则氧气的含量需要在48%~49%,分析坐标,可知道温度大约在82℃左右;
(7)采取“半值法”探究能减少实验次数,实际上就是通过实验数据的分析,减少不必要的实验,第二组实验若按②、③的编号顺序进行实验,即可确定下一组实验收集的氧气占容积的体积分数应在33%~35%之间,从而省去编号①、④、⑤的实验.
故答案为:(1)、高锰酸钾→锰酸钾+二氧化锰+氧气;
(2)、分液漏斗能够控制反应的发生;催化;
(3)、否;
(4)、21%;
(5)、35%; 49%(计算结果保留整数);
(6)、82;
(7)、①、④、⑤.
点评:本题考查的是氧气的制取装置装置的选择、验满方法、空气中氧气的含量和有关的计算,综合性比较强,要理解应用,综合把握.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目