题目内容
【题目】一定质量的锌、铁分别和等质量的相同盐酸反应,产生氢气质量与时间的关系如下图所示,下列说法不正确的是( )
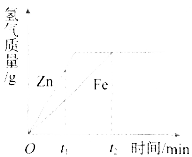
A.t1时,产生氢气的质量锌比铁大
B.t1时,产生氢气的速率锌比铁大
C.t2时,参加反应锌的质量与铁相等
D.t2时,锌、铁消耗的盐酸质量相等
【答案】C
【解析】此题考查金属与酸的反应以及对图像的分析能力.观察图像可知,t1min时,锌产生氢气的质量比铁的大.且锌的直线比铁的直线陡,说明锌产生氢气的速率比铁的大,则A、B正确;t2min时,生成氢气的质量相等,根据化学方程式Fe+2HCl=FeCl2+H2↑、Zn+2HCl=ZnCl2+H2↑可知,锌和铁消耗的盐酸的质量相等,但参加反应的锌和铁的质量不相等,则C错,D正确.

练习册系列答案
相关题目