题目内容
(2011?鄂尔多斯)请你结合下列实验装置回答有关问题: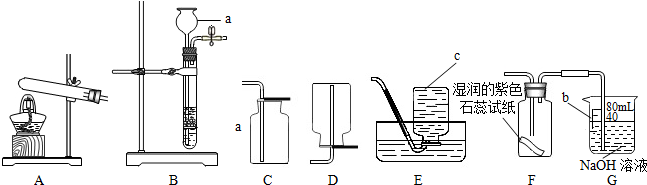
(1)写出标号仪器的名称:a
(2)实验室若用A装置制取氧气,则发生反应的化学方程式为
(3)实验室用块状固体亚硫酸钠与浓硫酸反应制取二氧化硫气体,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑,已知SO2气体密度比空气大,有毒,能与水反应生成亚硫酸.根据以上事实推断:实验室制取SO2气体应选用的发生装置是

(1)写出标号仪器的名称:a
长颈漏斗
长颈漏斗
,b烧杯
烧杯
(2)实验室若用A装置制取氧气,则发生反应的化学方程式为
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
(任写一个);收集氧气的装置应选用
| ||
| △ |
C或E
C或E
,(填字母)原因是氧气的密度比空气大,且氧气不易溶于水
氧气的密度比空气大,且氧气不易溶于水
.(3)实验室用块状固体亚硫酸钠与浓硫酸反应制取二氧化硫气体,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑,已知SO2气体密度比空气大,有毒,能与水反应生成亚硫酸.根据以上事实推断:实验室制取SO2气体应选用的发生装置是
B
B
,(填字母)用F、G装置收集SO2气体,F中的现象是石蕊试纸变成红色
石蕊试纸变成红色
,G中发生反应的化学方程式是SO2+2NaOH=Na2SO3+H2O
SO2+2NaOH=Na2SO3+H2O
.分析:(1)熟练掌握化学常见的仪器及用途;
(2)根据装置的特点选择的药品是加热氯酸钾和二氧化锰的混合物;根据氧气的密度和溶解性选择收集装置;
(3)根据反应物的状态和反应条件选择发生装置;根据二氧化硫的水溶液显酸性分析;二氧化硫与氢氧化钠反应生成盐和水.
(2)根据装置的特点选择的药品是加热氯酸钾和二氧化锰的混合物;根据氧气的密度和溶解性选择收集装置;
(3)根据反应物的状态和反应条件选择发生装置;根据二氧化硫的水溶液显酸性分析;二氧化硫与氢氧化钠反应生成盐和水.
解答:解:(1)a是长颈漏斗;b是烧杯;
(2)氯酸钾在二氧化锰的催化作用下,分解成氯化钾和氧气,反应的方程式为:2KClO3
2KCl+3O2↑;因为氧气的密度比空气大,且氧气不易溶于水,所以采用的收集方法是:C或E;
(3)根据信息提供的制取二氧化硫的反应物状态和反应条件属于固液常温型,所以选择的发生装置是:B;因为二氧化硫能够与水反应生成亚硫酸,显酸性,故能够使湿润的蓝色石蕊试纸变成红色;二氧化硫与氢氧化钠反应生成亚硫酸钠和水,反应的方程式为:SO2+2NaOH=Na2SO3+H2O.
故答案为:(1)长颈漏斗;烧杯;
(2)2KClO3
2KCl+3O2↑;C或E;氧气的密度比空气大,且氧气不易溶于水;
(3)B;石蕊试纸变成红色;SO2+2NaOH=Na2SO3+H2O.
(2)氯酸钾在二氧化锰的催化作用下,分解成氯化钾和氧气,反应的方程式为:2KClO3
| ||
| △ |
(3)根据信息提供的制取二氧化硫的反应物状态和反应条件属于固液常温型,所以选择的发生装置是:B;因为二氧化硫能够与水反应生成亚硫酸,显酸性,故能够使湿润的蓝色石蕊试纸变成红色;二氧化硫与氢氧化钠反应生成亚硫酸钠和水,反应的方程式为:SO2+2NaOH=Na2SO3+H2O.
故答案为:(1)长颈漏斗;烧杯;
(2)2KClO3
| ||
| △ |
(3)B;石蕊试纸变成红色;SO2+2NaOH=Na2SO3+H2O.
点评:本题考查了常见气体的制取和收集,并在已有知识的基础上进行拓展考查二氧化硫的制取和性质,能够考查学生的思维运用能力.

练习册系列答案
相关题目