题目内容
【题目】水垢的主要成分是碳酸钙和氢氧化镁,用酸可以清除水垢.某课外小组为了测定水垢中碳酸钙的含量,将过量的稀盐酸加入到200克水垢中,将产生的二氧化碳气体通入到足量的NaOH溶液,同时测得3分钟内NaOH溶液质量的增加情况,结果表示如下:
(假设产生的CO2气体全部被吸收)
时间/S | 0 | 30 | 60 | 90 | 120 | 150 | 180 |
增加的质量/g | 0 | 30 | 50 | 60 | 66 | 66 | 66 |
试回答下列问题
(1)实验中一共产生了克CO2气体.
(2)在图上画出产生的气体随时间变化的曲线.
(3)计算水垢中碳酸钙的质量分数,补齐计算步骤
(用到的相对原子质量为C﹣12 O﹣16)
解:设水垢样品中碳酸钙的质量为x
写化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑
求相对分子质量:100
物质的实际质量:x
列比例式计算:100:x=:
解方程求X:x=
求质量分数:求解出的x除以水垢样品总质量,乘以100%![]() ×100%=
×100%=
答:水垢中碳酸钙的质量分数为 .
【答案】
(1)66
(2)

(3)44;66;44;66;75%;75%
【解析】(1)由表中信息可知,生成二氧化碳质量是66g,(2)画图如下所示: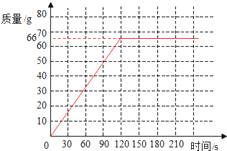
(3)设碳酸钙质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 66g
则 ![]() =
= ![]() ,解得x=150g,水垢中碳酸钙的质量分数为:
,解得x=150g,水垢中碳酸钙的质量分数为: ![]() ×100%=75%,
×100%=75%,
【考点精析】利用根据化学反应方程式的计算对题目进行判断即可得到答案,需要熟知各物质间质量比=系数×相对分子质量之比.

 阅读快车系列答案
阅读快车系列答案【题目】苯(C6H6)是一种重要的有机溶剂,它的部分同系列物质如下:
碳原子数 | 6 | 7 | 8 | 9 | 10 |
化学式 | C6H6 | C7H8 | X | C9H12 | Cl0H14 |
(1)比较归纳是学好化学的重要方法.据表推测:
①X的化学式为 .
②上述物质的共同特点有(写出一条即可).
(2)在C6H6中,C与H的质量比为 , 碳元素的质量分数为 .