题目内容
 如图所示,是A、B、C三种固体物质的溶解度曲线.
如图所示,是A、B、C三种固体物质的溶解度曲线.请据图回答下列问题:
(1)t1℃时,溶解度最大的物质是
A
A
(填序号).(2)t2℃时,A物质饱和溶液的质量分数为
20%
20%
;要配制100克t2℃A的饱和溶液,需要A20
20
克,需用100
100
(100毫升、50毫升)量筒量取80
80
毫升水,所需要的玻璃仪器除量筒、胶头滴管、烧杯外还需要玻璃棒
玻璃棒
.分析:(1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)饱和溶液中溶质的质量分数的计算式
×100%,并结合该温度下A的溶解度分析解答,配制溶液选取量筒遵循‘一次接近’的原则,并据配制溶液所需仪器分析解答.
(2)饱和溶液中溶质的质量分数的计算式
| 溶解度 |
| 溶解度+100g |
解答:解:(1)由图可知:t1℃时,溶解度最大的物质是 A;
(2)t2℃时,A物质的溶解度是25g,据饱和溶液中溶质的质量分数可知A饱和溶液的质量分数为
×100%=20%;要配制100克t2℃A的饱和溶液,需要A
×100g=20克,则需要水的质量是100g-20g=80g,合80mL,所以需用 100毫升、50毫升量筒量取80毫升水,所需要的玻璃仪器除量筒、胶头滴管、烧杯外,还需要玻璃棒;
故答案为:(1)A;(2)20%;20;100毫升;80;玻璃棒.
(2)t2℃时,A物质的溶解度是25g,据饱和溶液中溶质的质量分数可知A饱和溶液的质量分数为
| 25g |
| 125g |
| 25g |
| 125g |
故答案为:(1)A;(2)20%;20;100毫升;80;玻璃棒.
点评:掌握溶液的配制、溶解度概念、溶质的质量分数计算等知识才能正确分析解答该题.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
如图所示,是a、b两种固体物质的溶解度曲线.下列说法错误的是( )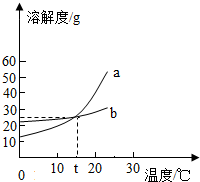

| A、在t℃时,a、b的饱和溶液中溶质的质量分数相同 | B、a的溶解度大于b的溶解度 | C、当a中含有少量b时,可以用结晶法提纯 | D、a和b都属于易溶物质 |
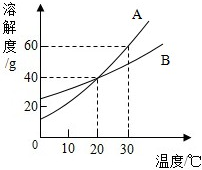 如图所示,是A、B两种固体物质的溶解度曲线.下列说法错误的是( )
如图所示,是A、B两种固体物质的溶解度曲线.下列说法错误的是( )| A、在30℃时,A物质的溶解度是60g | B、A的溶解度大于B的溶解度 | C、在20℃时,A、B的饱和溶液中溶质的质量分数相同 | D、A和B都属于易溶物质 |
 16、如图所示,是A、B两种固体物质的溶解度曲线,请回答下列问题:
16、如图所示,是A、B两种固体物质的溶解度曲线,请回答下列问题: 如图所示,是A、B、C三种固体物质的溶解度曲线.请据图回答下列问题:
如图所示,是A、B、C三种固体物质的溶解度曲线.请据图回答下列问题: