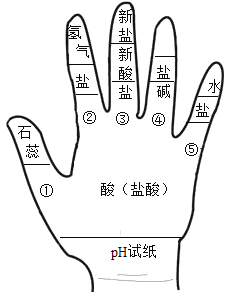
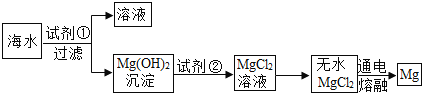
题目内容
日常使用的金属材料,大多数属于合金。黄铜是以锌作主要添加元素的铜合金,可用于武器制造。将22g弹壳(只含有锌和铜)放在盛有100g稀硫酸(足量)的烧杯中,当弹壳不再溶解后,烧杯中混合物的质量是121.8g。计算:
(1)产生氢气的质量 g。
(2)弹壳中铜的质量。
(3)反应后所得溶液中ZnSO4的质量分数(计算结果保留一位小数)。
练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案
相关题目
已知金属锰(Mn) 的活动性位于铝和锌之间,请预测硫酸锰(MnSO4)的化学性质,说明预测的依据,并设计实验验证。经查阅资料,锰的化合物相关性质如下:
物质 | MnO | Mn(OH)2 | MnCl2 | Mn(NO3)2 | MnSO4 | MnCO3 |
在水中的溶解性 | 不溶于水的草绿色粉末 | 难溶于水的白色固体 | 可溶于水形成淡红色溶液 | 溶于水形成淡红色溶液 | 溶于水形成淡红色溶液 | 难溶于水的粉红色固体 |
限选试剂:MnSO4溶液、(NH4)2CO3溶液、Na2SO4溶液、BaCl2溶液、NaOH溶液、稀盐酸、镁条、铜片。
预测 | 预测的依据 | 验证预测的实验操作与预期现象 |
①能够与含Ba2+的可溶性盐反应 | MnSO4溶液中含 | 取少量MnSO4溶液于试管中,_____,如果观察到_____,则预测成立。 |
②能够与_____(填物质类别)反应 | _____。 | 取少量MnSO4溶液于试管中,_____,如果观察到_____,则预测成立。 |
③能够与_____(填物质类别)反应 | _____。 | 取少量MnSO4溶液于试管中,_____,如果观察到_____,则预测成立。 |


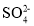 ,BaSO4难溶于水。
,BaSO4难溶于水。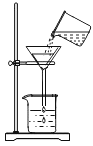 过滤河水 B.
过滤河水 B.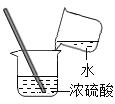 稀释浓硫酸
稀释浓硫酸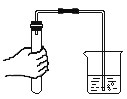 检查气密性 D.
检查气密性 D. 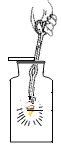 铁丝燃烧
铁丝燃烧