题目内容
【题目】如图一所示,点燃蜡烛,用蜡烛的火焰加热铜丝,2﹣3分钟后,观察到白磷燃烧,写出反应的化学方程式 , 铜丝的作用是 . 接着,红磷被燃烧的白磷引燃并延烧,产生白烟,此时熄灭蜡烛,向下用力使燃烧匙的勺子位于瓶体第1与第2等分线标记之间(如图二),此操作的目的是 . 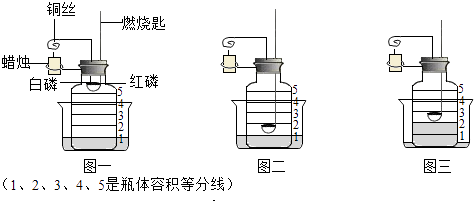
当燃烧匙内燃烧的磷火焰熄灭后,可观察到烧杯内的液面逐渐下降;待瓶体内的气体完全冷却到室温时,瓶体内的液面上升至瓶体第2等分线(如图三所示).由此说明:约占空气体积的 ![]() .如果该瓶体原来是装米醋的无色玻璃瓶,要达到上述实验效果应先对米醋瓶进行的加工是 .
.如果该瓶体原来是装米醋的无色玻璃瓶,要达到上述实验效果应先对米醋瓶进行的加工是 .
【答案】4P+5O2 ![]() 2P2O5;引燃白磷;充分消耗瓶内的氧气;氧气;将瓶底去
2P2O5;引燃白磷;充分消耗瓶内的氧气;氧气;将瓶底去
【解析】解:白磷能与氧气反应生成五氧化二磷,铜丝具有导电性,能导热从而引燃白磷,向下用力使燃烧匙的勺子位于瓶体第1与第2等分线标记之间的目的是充分消耗瓶内的氧气,以使测定的结果更接近真实值;待瓶体内的气体完全冷却到室温时,瓶体内的液面上升至瓶体第2等分线,说明氧气约占空气总体积的五分之一,如果该瓶体原来是装米醋的无色玻璃瓶,需要在实验之前将瓶底去掉,故填:4P+5O2 ![]() 2P2O5,引燃白磷,充分消耗瓶内的氧气,氧气,将瓶底去.
2P2O5,引燃白磷,充分消耗瓶内的氧气,氧气,将瓶底去.
根据测定空气中氧气体积分数的原理分析,测定氧气体积分数时选择能与空气中氧气反应的物质,且生成物为固体,使得装置内因氧气反应消耗压强变小,再根据补充的水的体积确定氧气的体积。

【题目】许多金属氧化物对氯酸钾的分解有催化作用.分别用下列金属氧化物作催化 剂,氯酸钾开始反应和反应剧烈时的温度如下表所示:
三氧化二铁 | 三氧化二铝 | 氧化铜 | 二氧化锰 | |
开始反应 | 470℃ | 515℃ | 305℃ | 490℃ |
剧烈反应 | 490℃ | 540℃ | 350℃ | 545℃ |
实验室用氯酸钾制氧气,如果不用二氧化锰作催化剂,最好选用( )
A.三氧化二铁B.三氧化二铝C.氧化铜D.氧化锰