题目内容
医药上用的阿斯匹林的组成里含有4.5%的氢、35.5%的氧、60%的碳,它的式量为180.设阿斯匹林的化学式为CxHyOz,则x值为 ,y值为 ,z值为 .若将阿斯匹林在空气中完全燃烧,反应的化学方程式为: .
分析:根据题意,阿斯匹林的组成里含有4.5%的氢、35.5%的氧、60%的碳,它的式量为180.设阿斯匹林的化学式为CxHyOz,利用化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
阿司匹林在空气中完全燃烧,生成二氧化碳和水,写出反应的化学方程式即可.
阿司匹林在空气中完全燃烧,生成二氧化碳和水,写出反应的化学方程式即可.
解答:解:医药用的阿司匹林的组成为:含碳60%、氢4.5%、氧35.5%,其式量(即相对分子质量)为180.
则碳原子的相对原子质量质量之和为180×60%=108,12×x=108 x=9.
氢原子的相对原子质量质量之和为180×4.5%≈8,1×y=8,y=8.
氧原子的相对原子质量质量之和为180×35.5%≈64,16×z=64 z=4.
则阿司匹林的化学式为C9H8O4.
阿司匹林在空气中完全燃烧,生成二氧化碳和水,反应的化学方程式为C9H8O4+9O2
9CO2+4H2O.
故答案为:9;8;4;C9H8O4+9O2
9CO2+4H2O.
则碳原子的相对原子质量质量之和为180×60%=108,12×x=108 x=9.
氢原子的相对原子质量质量之和为180×4.5%≈8,1×y=8,y=8.
氧原子的相对原子质量质量之和为180×35.5%≈64,16×z=64 z=4.
则阿司匹林的化学式为C9H8O4.
阿司匹林在空气中完全燃烧,生成二氧化碳和水,反应的化学方程式为C9H8O4+9O2
| ||
故答案为:9;8;4;C9H8O4+9O2
| ||
点评:本题难度不大,考查同学们灵活运用化学式的有关计算、化学方程式的书写进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
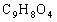 ,其相对分子质量为 ,由 种元素组成,其一个分子中由 个原子构成,碳、氢、氧元素的质量比为 ,碳元素的质量分数为 。
,其相对分子质量为 ,由 种元素组成,其一个分子中由 个原子构成,碳、氢、氧元素的质量比为 ,碳元素的质量分数为 。