题目内容
【题目】高氯酸(HClO4)和亚氯酸钠(NaClO2)在工业上有广泛的用途,其制备工艺流程如下:
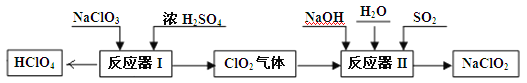
请回答下列问题:
(1)HClO4中Cl元素的化合价是 。
(2)反应器I中的生成物有HClO4、ClO2、Na2SO4、H2O,其中属于氧化物的是 。
(3)反应器II中发生反应的化学方程式为2ClO2+SO2+4NaOH=2NaClO2+X+2H2O,则X的化学式
是 。
【答案】(1)+7 (2)ClO2、H2O (3)Na2SO4
【解析】
试题分析:(1)根据元素化合价的一般规律:在化合物中,正负化合价的代数和为0,HClO4中H的化合价为+1,O的化合价为-2,故Cl元素的化合价是+7
(2)氧化物由两元素组成,其中一种为氧元素的化合物,HClO4、ClO2、Na2SO4、H2O,其中属于氧化物的是:ClO2、H2O
(3)根据质量守恒定律的微观解释,在化学反应前后,原子的种类、个数都不变,结合化学方程式:2ClO2+SO2+4NaOH=2NaClO2+X+2H2O,不难推出X的化学式是Na2SO4

练习册系列答案
相关题目
