题目内容
(2009?海门市模拟)滑石是矿石的一种,它与含有石棉成分的其它纹石共同埋藏在地下.滑石中主要成分的化学式为:Mg3Si4O10(OH)2,相对分子质量为378;石棉中主要成分的化学式为:Mg6Si4O10(OH)8.计算填空下列问题:
(1)Mg3Si4O10(OH)2中氢元素和氧元素的质量比是______;
(2)滑石和石棉中的主要成分的相对分子质量差为______;
(3)工业上提炼24gMg需要Mg3Si4O10(OH)2的质量______.
【答案】分析:(1)利用化学式Mg3Si4O10(OH)2,由元素相对原子质量及原子个数计算其中H、O元素质量比;
(2)利用化学式Mg3Si4O10(OH)2,由元素相对原子质量及原子个数计算相对分子质量,并与滑石的相对分子质量进行对比,计算出两物质相对分子质量差;
(3)根据化学式Mg3Si4O10(OH)2,利用元素质量÷该元素在化合物中的质量分数=所需该物质的质量,完成工业上提炼24gMg需要Mg3Si4O10(OH)2的质量的计算.
解答:解:(1)Mg3Si4O10(OH)2中氢元素和氧元素的质量比=(1×2):(16×12)=1:96;
(2)石棉Mg6Si4O10(OH)8的相对分子质量=24×6+28×4+16×18+1×8=552;与滑石Mg3Si4O10(OH)2的相对分子质量378的差=552-378=174;
(3)含24gMg的Mg3Si4O10(OH)2的质量=24g÷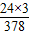 ×100%=126g;
×100%=126g;
故答案为:(1)1:96;(2)174;(3)126g.
点评:根据一定量化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数,已知等式中任意两个量,可计算出第三个量.
(2)利用化学式Mg3Si4O10(OH)2,由元素相对原子质量及原子个数计算相对分子质量,并与滑石的相对分子质量进行对比,计算出两物质相对分子质量差;
(3)根据化学式Mg3Si4O10(OH)2,利用元素质量÷该元素在化合物中的质量分数=所需该物质的质量,完成工业上提炼24gMg需要Mg3Si4O10(OH)2的质量的计算.
解答:解:(1)Mg3Si4O10(OH)2中氢元素和氧元素的质量比=(1×2):(16×12)=1:96;
(2)石棉Mg6Si4O10(OH)8的相对分子质量=24×6+28×4+16×18+1×8=552;与滑石Mg3Si4O10(OH)2的相对分子质量378的差=552-378=174;
(3)含24gMg的Mg3Si4O10(OH)2的质量=24g÷
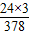 ×100%=126g;
×100%=126g;故答案为:(1)1:96;(2)174;(3)126g.
点评:根据一定量化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数,已知等式中任意两个量,可计算出第三个量.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
(2009?海门市模拟)某实验小组利用下图装置对实验室制取CO2的速率快慢进行了研究.他们实验时所用的试剂和使用的反应条件如下表所示:
写出实验过程中发生反应的化学方程式______.
(1)实验小组同学设计的实验方案部分如下表,请根据表中信息帮助填写完整:
(2)实验探究时,他们每次收集CO2气体均为40mL,则实验中他们还应记录的实验数据是:______.
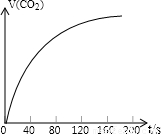
右图是根据某次实验数据作出的CO2和时间变化的关系曲.
请分析在80秒以后,产生CO2逐渐减慢的可能原因:
______.

| 盐酸 | 大理石 | 温度条件 |
| 5% | 细颗粒 | 20℃ |
| 10% | 粗颗粒 | 40℃ |
| 每次用量均 | 每次用量均5g |
(1)实验小组同学设计的实验方案部分如下表,请根据表中信息帮助填写完整:
| 实验编号 | 温度 | 大理石规格 | HCl浓度 | 探究目的 |
| ① | 20℃ | 粗颗粒 | 5% | (I)实验①和②探究浓度对反应快慢的影响; (II)实验②和______探究温度对反应快慢的影响; (III)实验______和______探究大理石粗、细对反应快慢的影响. |
| ② | 20℃ | 粗颗粒 | ______ | |
| ③ | ______ | 细颗粒 | 5% | |
| ④ | 40℃ | ______ | 10% |
右图是根据某次实验数据作出的CO2和时间变化的关系曲.
请分析在80秒以后,产生CO2逐渐减慢的可能原因:
______.

