题目内容
【题目】在人们担心化石能源被耗尽时,科学家发现海底埋藏着大量可燃烧的“冰”——“可燃冰”。可燃冰的外观像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等气体。可燃冰在低温和高压条件下形成,1体积可燃冰可储载100~200倍体积的甲烷气体,具有能量高,燃烧值大等优点。可燃冰将成为未来新能源。目前,我国在可燃冰的开采技术上处于世界领先水平。
回答下列问题:
(1)可燃冰属于_____________。(填字母序号)
A 纯净物 B 混合物
(2)甲烷在空气中完全燃烧的化学方程式为__________________________________。
(3)甲烷中氢为+1价,碳为________价。
(4)从环境保护的角度考虑,下列燃料中最理想的是_________ 。(填字母序号)
A 氢气 B 可燃冰 C 酒精 D 汽油
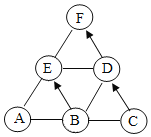
(5)甲烷重整可以得到合成气体,其反应的微观示意图如图:
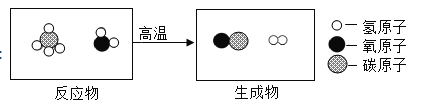
写出上述反应的化学方程式:_____________________。
(6)用不同催化剂可使合成气体合成不同的物质。下列物质仅以合成气为原料不可能得到的是_____(填序号)。
A 甲醛(CH2O) B 甲醇(CH3OH) C 尿素[CO(NH2)2]
【答案】B ![]() -4 A CH4+H2O
-4 A CH4+H2O![]() CO+3H2↑ C
CO+3H2↑ C
【解析】
(1)可燃冰主要成分是甲烷,还含有一些杂质,是混合物。故选B。
(2)甲烷在空气中完全燃烧生成二氧化碳和水,化学方程式为![]() ,
,
(3)甲烷的化学式是CH4,氢元素显+1价,设碳元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(+1)×4=0,则x=-4价。
(4)A、氢气燃烧生成水,对环境没有污染,符合题意;
B、可燃冰燃烧释放出二氧化碳等气体,会造成温室效应,不符合题意;
C、酒精燃烧释放出二氧化碳等气体,会造成温室效应,不符合题意;
D、汽油燃烧释放出二氧化碳等气体,会造成温室效应,产生的二氧化硫气体会造成酸雨,不符合题意。故选A。
(5)由微观反应示意图可知,该反应是甲烷与水蒸气在高温的条件下反应生成一氧化碳和氢气,化学反应方程式为:CH4+H2O![]() CO+3H2↑;
CO+3H2↑;
(6)由质量守恒定律可知,反应前后原子的种类及数目不变,在反应前的物质中含有碳、氢、氧三种元素,不含有氮元素,可以合成甲醛、甲醇,但不能合成尿素。故选C。

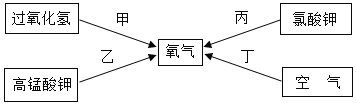
【题目】对空气中氧气含量测定的再认识。
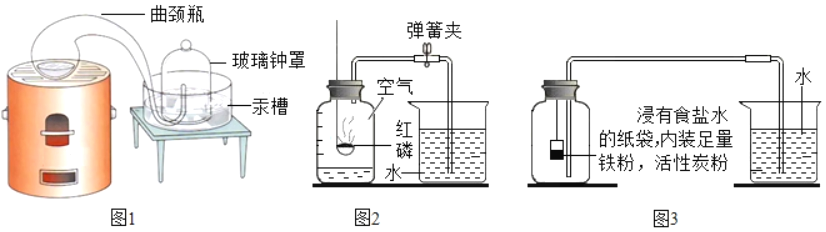
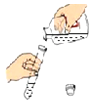
(经典赏析)用图1装置测定空气中氧气含量的科学家是_____。
(1)该实验中选择汞为实验药品,把它放在密闭的容器里连续加热12天,发现一部分银白色的液态汞变成红色粉末,同时容器里空气的体积差不多减少![]() ,对应观察到的现象为_____。
,对应观察到的现象为_____。
(2)该实验中使用汞的缺点是_____。
A 汞有毒,实验过程中不安全 B 汞为液态,在汞槽中起到液封作用
C 生成的化合物加热分解又能得到汞和氧气 D 实验时间太长
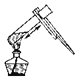
(实验回顾)图2是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)写出红磷燃烧的文字表达式:_____。
(2)实验原理:由于红磷燃烧消耗空气中氧气,使瓶内减小,烧杯中水倒吸到集气瓶中。用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
(3)对该实验认识正确的是_____。
A 红磷燃烧产生大量白色的烟雾
B 红磷的用量不足会导致测定氧气体积含量偏大
C 红磷燃烧以后,须冷却到室温方可打开止水夹
D 该实验可说明氮气难溶于水
(问题提出)某小组同学多次实验发现,集气瓶内上升的水面始终小于理论值。经查阅资料知:
燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测得结果与理论值相差较大。
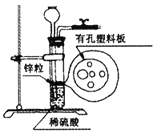
(实验改进)Ⅰ.根据铁丝在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计如图3实验装置,再次测定空气中氧气含量,装置中的食盐水和活性炭会加速铁生锈。
Ⅱ.测得实验数据如表:
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
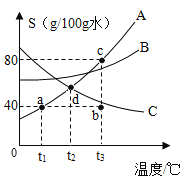
(1)根据表中数据计算,改进实验后测得的空气中氧气体积分数是_____。(消耗的水的体积忽略不计,计算结果精确到0.1%)。
(2)实验反思:从原理的角度分析,与红磷燃烧法相比,用铁丝生锈法测定空气中氧气含量的优点是_____。
(经典再识)科学家选择汞作为药品也有优点:汞的沸点为356.6℃,加热时源源不断气化的汞原子和空气中的氧分子发生的反应属于气相反应,反应可以达到完全,因此汞_____(填“能”或“不能”)将密闭容器内的氧气几乎耗尽!