题目内容
“9?11事件”发生不久,在美国又出现了炭疽热病,此病是由一种炭疽杆菌引发的急性传染病,致死率高达25%到60%.治疗炭疽热的常用抗生素为环丙沙星,其化学式为C17H18FN3O3.它由________种元素组成,每个分子中含有________个原子,其相对分子质量为________,其中质量分数最大的元素为________,质量分数为________.
5 42 373 碳元素 54.7%
分析:根据环丙沙星的化学式C17H18FN3O3,我们可以获得的信息有:环丙沙星由五种元素组成;每个分子中含有42个原子;它的相对分子质量是各个原子的相对原子质量的总和;还可以根据化学式求元素的质量分数.
解答:环丙沙星由五种元素组成;每个分子中含有42个原子;它的相对分子质量=12×17+18+19+14×3+16×3=373,其中质量分数最大的元素碳元素,碳的质量分数=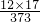 ×100%=54.7%;故答案为:5;42;373;碳元素;54.7%
×100%=54.7%;故答案为:5;42;373;碳元素;54.7%
点评:本考点考查了化学式表示的意义和有关的计算,元素符号、化学式、化学方程式等化学用语表示的意义是中考的重要考点之一,要加强练习,理解应用.本考点主要出现在选择题和填空题中.
分析:根据环丙沙星的化学式C17H18FN3O3,我们可以获得的信息有:环丙沙星由五种元素组成;每个分子中含有42个原子;它的相对分子质量是各个原子的相对原子质量的总和;还可以根据化学式求元素的质量分数.
解答:环丙沙星由五种元素组成;每个分子中含有42个原子;它的相对分子质量=12×17+18+19+14×3+16×3=373,其中质量分数最大的元素碳元素,碳的质量分数=
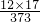 ×100%=54.7%;故答案为:5;42;373;碳元素;54.7%
×100%=54.7%;故答案为:5;42;373;碳元素;54.7%点评:本考点考查了化学式表示的意义和有关的计算,元素符号、化学式、化学方程式等化学用语表示的意义是中考的重要考点之一,要加强练习,理解应用.本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目