题目内容
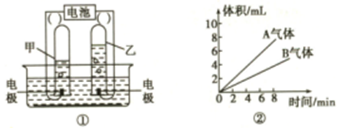
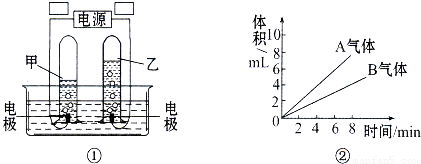
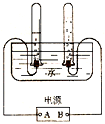 如图是电解水的实验装置示意图:
如图是电解水的实验装置示意图:
(1)判断电源的正负极.正极为:______(填A或B).
(2)与负极极相连的试管中产生的气体是______气;产生的氢气和氧气的体积比为______,质量比为______.
(3)在实验中加入稀硫酸或者氢氧化钠的原因是______.
(4)该反应的化学表达式是______.
(5)该反应可以得出的结论有:
①水是由______组成;
②在化学变化中,______可以再分,而______不可以再分.
解:(1)气体少的试管为氧气,连接的电极为正极,故:B为正极;
(2)A电极产生的气体较多,与A电极相连的试管产生的是氢气,产生氢气与氧气的体积比为2:1,质量比为1:8;
(3)加入稀硫酸或者氢氧化钠的原因是增强水的导电性,也是为了加快电解速度;
(4)反应的化学表达式是 2H2O 2H2↑+O2↑;
2H2↑+O2↑;
(5)由水通电可以分解出氢气和氧气,可知水是由氢、氧两种元素组成的化合物;在水分解的过程中水分子被分开成为氢氧两种原子,两种原子再重新组合成为氢氧两种分子,所以可知分子在化学变化中可分,原子不可分.
故答案为:
(1)B;
(2)氢;2:1;1:8;
(3)增强水导电性;
(4)2H2O 2H2↑+O2↑;
2H2↑+O2↑;
(5)①氢元素、氧元素;②分子,原子.
分析:(1)根据试管内气体的多少判断电极的正负;
(2)电解水时,与正极相连的试管生成的气体是氧气,较少.与负极相连的试管生成的是氢气,较多.氢气的体积是氧气体积的2倍;
(3)加入稀硫酸或者氢氧化钠的原因是增强水的导电性,也是为了加快电解速度;
(4)书写化学表达式时要注意反应条件与气体生成号;
(5)水通电可以分解出氢气和氧气,可知水是由氢、氧两种元素组成,一个水分子是由两个氢原子和一个氧原子构成;而水中没有氢气、氧气和氢分子,据此依据反应的特征结合化学变化的实质分析问题即可.
点评:通过电解水的实验,可以证明水由H、O元素组成,根据电解生成氢气、氧气体积比2:1,可推导水分子中氢、氧原子个数比为2:1.
(2)A电极产生的气体较多,与A电极相连的试管产生的是氢气,产生氢气与氧气的体积比为2:1,质量比为1:8;
(3)加入稀硫酸或者氢氧化钠的原因是增强水的导电性,也是为了加快电解速度;
(4)反应的化学表达式是 2H2O
 2H2↑+O2↑;
2H2↑+O2↑;(5)由水通电可以分解出氢气和氧气,可知水是由氢、氧两种元素组成的化合物;在水分解的过程中水分子被分开成为氢氧两种原子,两种原子再重新组合成为氢氧两种分子,所以可知分子在化学变化中可分,原子不可分.
故答案为:
(1)B;
(2)氢;2:1;1:8;
(3)增强水导电性;
(4)2H2O
 2H2↑+O2↑;
2H2↑+O2↑;(5)①氢元素、氧元素;②分子,原子.
分析:(1)根据试管内气体的多少判断电极的正负;
(2)电解水时,与正极相连的试管生成的气体是氧气,较少.与负极相连的试管生成的是氢气,较多.氢气的体积是氧气体积的2倍;
(3)加入稀硫酸或者氢氧化钠的原因是增强水的导电性,也是为了加快电解速度;
(4)书写化学表达式时要注意反应条件与气体生成号;
(5)水通电可以分解出氢气和氧气,可知水是由氢、氧两种元素组成,一个水分子是由两个氢原子和一个氧原子构成;而水中没有氢气、氧气和氢分子,据此依据反应的特征结合化学变化的实质分析问题即可.
点评:通过电解水的实验,可以证明水由H、O元素组成,根据电解生成氢气、氧气体积比2:1,可推导水分子中氢、氧原子个数比为2:1.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
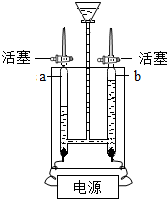 水是宝贵的自然资源.
水是宝贵的自然资源.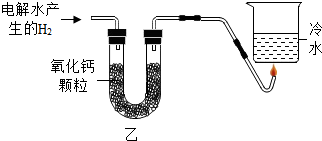
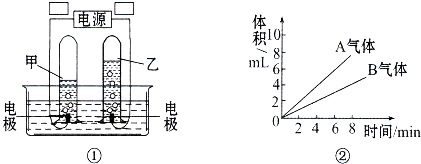
 水是宝贵的自然资源.
水是宝贵的自然资源.