题目内容
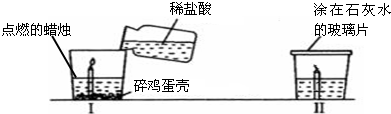
某同学在家做了如图所示的小实验,根据图示实验回答下列问题: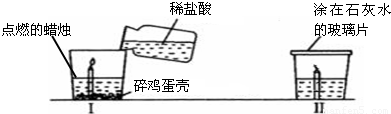
(1)鸡蛋壳内含碳酸钙,实验Ⅰ观察到的现象是①鸡蛋壳表面有气泡产生;② ,由此得出有关CO2性质的结论是 ,并依此性质确定CO2一个主要用途是 .
(2)蜡烛熄灭后,在玻璃杯口迅速盖一块涂蘸有石灰水的玻璃片.Ⅱ观察到的现象是 ,有关化学方程式为 .据Ⅱ中实验,能否证明蜡烛中含有碳元素? .为什么? .
【答案】分析:(1)根据二氧化碳的性质分析;
(2)依据碳酸盐和酸反应能生成二氧化碳,生成的二氧化碳能使澄清石灰水变浑浊进行判断,并书写方程式;根据元素在化学反应前后的质量不变分析使石灰水变浑浊的来源;
解答:解:(1)鸡蛋壳的主要成分是碳酸钙,可以与盐酸反应生成二氧化碳气体,而二氧化碳的密度比空气大,二氧化碳不能燃烧也不能支持燃烧,随着反应的进行,二氧化碳逐渐增多,淹没蜡烛,会看到蜡烛熄灭;因此二氧化碳可以用于灭火;
故答案为:蜡烛过一会熄灭;二氧化碳的密度比空气大,二氧化碳不能燃烧也不能支持燃烧;用于灭火;
(2)鸡蛋壳的主要成分是碳酸钙,可以与盐酸反应生成二氧化碳气体,生成的二氧化碳气体能和澄清石灰水反应生成不溶于水的白色固体碳酸钙而使溶液变浑浊;反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;根据质量守恒定律中化学反应前后元素的种类不变,蜡烛燃烧会产生二氧化碳能使澄清的石灰水变浑浊,但鸡蛋壳反应也会产生二氧化碳,故无法确定二氧化碳的来源.
故答案为:
(1)蜡烛过一会熄灭;二氧化碳的密度比空气大,二氧化碳不能燃烧也不能支持燃烧;用于灭火;
(2)澄清的石灰水变浑浊; Ca(OH)2+CO2=CaCO3↓+H2O 不能 因为不能确定使石灰水变浑浊的二氧化碳是来自鸡蛋壳反应产生的还是来自蜡烛燃烧产生的.
点评:本题考查了碳酸盐与酸的反应生成的二氧化碳的有关性质、化学方程式的书写及质量是定律的运用,这些重点内容要熟练掌握并灵活应用.
(2)依据碳酸盐和酸反应能生成二氧化碳,生成的二氧化碳能使澄清石灰水变浑浊进行判断,并书写方程式;根据元素在化学反应前后的质量不变分析使石灰水变浑浊的来源;
解答:解:(1)鸡蛋壳的主要成分是碳酸钙,可以与盐酸反应生成二氧化碳气体,而二氧化碳的密度比空气大,二氧化碳不能燃烧也不能支持燃烧,随着反应的进行,二氧化碳逐渐增多,淹没蜡烛,会看到蜡烛熄灭;因此二氧化碳可以用于灭火;
故答案为:蜡烛过一会熄灭;二氧化碳的密度比空气大,二氧化碳不能燃烧也不能支持燃烧;用于灭火;
(2)鸡蛋壳的主要成分是碳酸钙,可以与盐酸反应生成二氧化碳气体,生成的二氧化碳气体能和澄清石灰水反应生成不溶于水的白色固体碳酸钙而使溶液变浑浊;反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;根据质量守恒定律中化学反应前后元素的种类不变,蜡烛燃烧会产生二氧化碳能使澄清的石灰水变浑浊,但鸡蛋壳反应也会产生二氧化碳,故无法确定二氧化碳的来源.
故答案为:
(1)蜡烛过一会熄灭;二氧化碳的密度比空气大,二氧化碳不能燃烧也不能支持燃烧;用于灭火;
(2)澄清的石灰水变浑浊; Ca(OH)2+CO2=CaCO3↓+H2O 不能 因为不能确定使石灰水变浑浊的二氧化碳是来自鸡蛋壳反应产生的还是来自蜡烛燃烧产生的.
点评:本题考查了碳酸盐与酸的反应生成的二氧化碳的有关性质、化学方程式的书写及质量是定律的运用,这些重点内容要熟练掌握并灵活应用.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
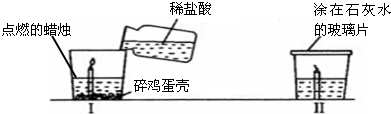
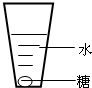 某同学在家做了如图所示实验:在一个玻璃容器中加入100mL水,向水中放入一块糖,在容器外壁沿液面画一条水平线,过一会儿发现糖块溶解,液面比原来水平线低了.通过这一现象请你推测分子具有哪些性质?选择其中一点性质,重新设计一个实验进行探究.
某同学在家做了如图所示实验:在一个玻璃容器中加入100mL水,向水中放入一块糖,在容器外壁沿液面画一条水平线,过一会儿发现糖块溶解,液面比原来水平线低了.通过这一现象请你推测分子具有哪些性质?选择其中一点性质,重新设计一个实验进行探究.