题目内容
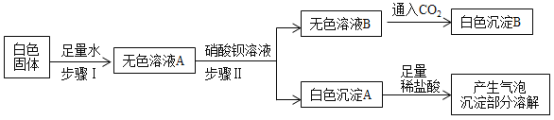
【题目】有一包白色固体样品,可能含有NaOH、Na2CO3、K2SO4、NaCl中的一种或几种,为确定其组成,进行如下实验:
①步骤II中发生的化学反应方程式_____(写一条即可)。
②无色溶液B中的溶质一定有_____。
③分析上述实验过程,仍无法确定的物质是_____。
④若要进一步确定样品的组成,还需进行的实验操作是_____。
【答案】![]() (或
(或![]() ) 硝酸钡和氢氧化钠 氯化钠 取适量B溶液于试管中,加入足量稀硝酸,滴加硝酸银溶液,如果产生白色沉淀,说明含有氯化钠,反之则不含有氯化钠
) 硝酸钡和氢氧化钠 氯化钠 取适量B溶液于试管中,加入足量稀硝酸,滴加硝酸银溶液,如果产生白色沉淀,说明含有氯化钠,反之则不含有氯化钠
【解析】
硝酸钡和硫酸钠反应生成硫酸钡沉淀和硝酸钠,和碳酸钠反应生成碳酸钡沉淀和硝酸钠,硫酸钡不溶于稀盐酸,碳酸钡能溶于稀盐酸。步骤II后得到白色沉淀A和无色溶液B,白色沉淀A加足量稀盐酸,产生气泡、部分沉淀溶解,则样品一定有Na2CO3、K2SO4,无色溶液B中通入二氧化碳产生白色沉淀,是因为氢氧化钠和二氧化碳反应生成的碳酸钠和过量的硝酸钡反应生成白色沉淀碳酸钡,B中溶质一定有硝酸钡和氢氧化钠;不能确定是否含氯化钠;
①步骤Ⅱ中硝酸钡和硫酸钠反应生成硫酸钡沉淀和硝酸钠,和碳酸钠反应生成碳酸钡沉淀和硝酸钠,反应的化学方程式:![]() 、
、![]() 。
。
②无色溶液B中通入二氧化碳产生白色沉淀,是因为氢氧化钠和二氧化碳反应生成的碳酸钠和过量的硝酸钡反应生成白色沉淀碳酸钡,B中溶质一定有硝酸钡和氢氧化钠。
③分析上述实验过程,仍无法确定的物质是氯化钠。
④若要进一步确定样品的组成,还需进行的实验操作是:取适量B溶液于试管中,加入足量稀硝酸,滴加硝酸银溶液,如果产生白色沉淀,说明含有氯化钠,反之则不含有氯化钠。

 阅读快车系列答案
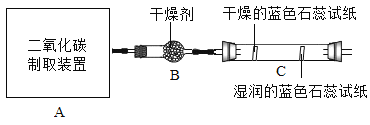
阅读快车系列答案【题目】制造物质、研究物质 小博同学想组装一套能控制反应速率,获得平稳气流的实验室制取二氧化碳装置,则发生装置应选择_________ (填序号)装置,利用装置 E 收集二氧化碳,气体应从_________(填“a”或“b”)端通入;
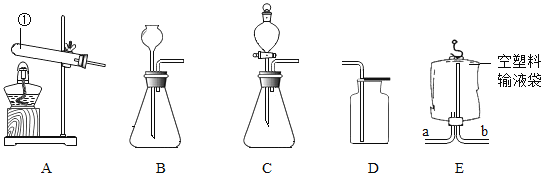
小博同学运用所制得的二氧化碳采用用对比实验方法探究二氧化碳的性质,请根据下列实验要求回答相关问题:
实验一 | 实验二 |
|
|
实验一:振荡 3 个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为 A>B>C, 其中 B 瓶石灰水变浑浊,此反应的化学方程式为_________; 对比_________瓶(选填“A”“B”或“C”)的塑 料瓶变瘪的程度,可证明 CO2 能与 NaOH 发生反应。
实验二:观察到 C 装置中发生的现象是:_________蓝色石蕊试纸_________;此实验可证明__________发生反应。