题目内容
用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如下图所示:
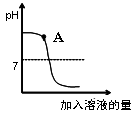
① 该实验是将 (填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
② A点溶液中的溶质为 。
③ 要测出反应过程中溶液的PH,应如何操作 。

① 该实验是将 (填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
② A点溶液中的溶质为 。
③ 要测出反应过程中溶液的PH,应如何操作 。
稀盐酸 氢氧化钠和氯化钠 用洁净干燥的玻璃棒蘸取待测液少量滴在pH试纸的中间,半分钟后将试纸呈现的颜色与标准比色卡进行对照,从而确定溶液的pH。
试题分析:刚开始溶液的pH大于7,所以是将稀盐酸加入氢氧化钠溶液中,A点时溶液呈碱性所以有氢氧化钠,又因为稀盐酸和氢氧化钠发生了反应生成氯化钠,所以此时溶质为氢氧化钠和氯化钠。测定溶液pH的操作为用洁净干燥的玻璃棒蘸取待测液少量滴在pH试纸的中间,半分钟后将试纸呈现的颜色与标准比色卡进行对照,从而确定溶液的pH。

练习册系列答案
相关题目

