题目内容
写出下列反应的化学方程式,并注明反应类型:(1)实验室用过氧化氢制氧气
(2)正常雨水的pH约为5.6
(3)铜丝浸入硝酸银溶液中
(4)氢氧化铝用于治疗胃酸过多
分析:(1)根据过氧化氢在二氧化锰的催化作用下会生成水和氧气进行分析,
(2)根据空气中的二氧化碳会溶于雨水形成碳酸来分析,
(3)根据铜的活动性排在银之前,会将银置换出来进行分析,
(4)根据胃酸的主要成分是碳酸,会与氢氧化铝发生中和反应来判断.根据反应物的种类判断反应的基本类型.
(2)根据空气中的二氧化碳会溶于雨水形成碳酸来分析,
(3)根据铜的活动性排在银之前,会将银置换出来进行分析,
(4)根据胃酸的主要成分是碳酸,会与氢氧化铝发生中和反应来判断.根据反应物的种类判断反应的基本类型.
解答:解:(1)过氧化氢在二氧化锰的催化作用下反应生成水和氧气.该反应的化学方程式为:2H2O2
2H2O+O2↑.该反应由一种物质反应生成两种物质,符合分解反应的概念,属于分解反应.
(2)正常雨水的pH约为5.6,说明雨水显酸性,雨水中含有酸,所含的酸是由二氧化碳与水化合生成碳酸造成的.该反应的化学方程式为:CO2+H2O=H2CO3.该反应由两种物质反应生成一种物质,符合化合反应的概念,属于化合反应.
(3)在金属活动性顺序表中铜排在银的前面,因此铜能将银从银的盐溶液中置换出来.因此,铜丝浸入硝酸银溶液中时,铜能与硝酸银反应生成银和硝酸铜.该反应的化学方程式为:Cu+2AgNO3=2Ag+Cu(NO3)2.该反应由一种单质与一种化合物反应生成另一种单质和另一种化合物,符合置换反应的概念,属于置换反应.
(4)氢氧化铝是碱,胃液中含有盐酸,氢氧化铝能与盐酸反应生成氯化铝和水.该反应的化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O.该反应由两种化合物相互交换成分形成两种新的化合物,符合复分解反应的概念,属于复分解反应.
故答案为:
(1)2H2O2
2H2O+O2↑;分解
(2)CO2+H2O=H2CO3;化合
(3)Cu+2AgNO3=2Ag+Cu(NO3)2;置换
(4)Al(OH)3+3HCl=AlCl3+3H2O;复分解
| ||
(2)正常雨水的pH约为5.6,说明雨水显酸性,雨水中含有酸,所含的酸是由二氧化碳与水化合生成碳酸造成的.该反应的化学方程式为:CO2+H2O=H2CO3.该反应由两种物质反应生成一种物质,符合化合反应的概念,属于化合反应.
(3)在金属活动性顺序表中铜排在银的前面,因此铜能将银从银的盐溶液中置换出来.因此,铜丝浸入硝酸银溶液中时,铜能与硝酸银反应生成银和硝酸铜.该反应的化学方程式为:Cu+2AgNO3=2Ag+Cu(NO3)2.该反应由一种单质与一种化合物反应生成另一种单质和另一种化合物,符合置换反应的概念,属于置换反应.
(4)氢氧化铝是碱,胃液中含有盐酸,氢氧化铝能与盐酸反应生成氯化铝和水.该反应的化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O.该反应由两种化合物相互交换成分形成两种新的化合物,符合复分解反应的概念,属于复分解反应.
故答案为:
(1)2H2O2
| ||
(2)CO2+H2O=H2CO3;化合
(3)Cu+2AgNO3=2Ag+Cu(NO3)2;置换
(4)Al(OH)3+3HCl=AlCl3+3H2O;复分解
点评:在解此类题时,首先分析物质的反应原理,然后根据方程式的书写规则进行书写,根据反应物的种类判断属于的反应类型.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
(2009?娄底)小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
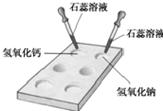
(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方 程式______.
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式______.
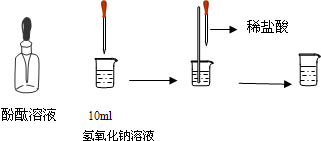
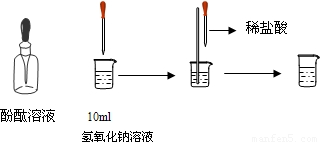
(4)如图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显______色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止.这一实验说明:酸与碱作用生成了盐和水,这一反应叫做______反应.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)?
①______
②______.
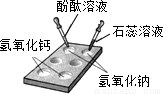
(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | ______ | ______ |
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式______.
(4)如图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显______色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止.这一实验说明:酸与碱作用生成了盐和水,这一反应叫做______反应.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)?
①______
②______.