题目内容
某温度下,将4克氯化钠加入到10克水中,充分搅拌后仍有0.4克固体不溶解.则该温度时,氯化钠的溶解度为
36g
36g
;将上述混合物过滤除去不溶物后,继续向滤液中滴加某浓度的硝酸银溶液,到不再产生沉淀时共用去硝酸银溶液105克.请计算该硝酸银溶液中溶质的质量分数.(NaCl+AgNO3═AgCl↓+NaNO3,结果保留整数)分析:某温度下,氯化钠在100g水中达到饱和状态时溶解的质量即为该温度下的溶解度;
根据化学方程式可以计算硝酸银的质量,进一步可以计算硝酸银溶液的质量分数.
根据化学方程式可以计算硝酸银的质量,进一步可以计算硝酸银溶液的质量分数.
解答:某温度下,10g水溶解3.6g氯化钠达到饱和状态,那么100g水中溶解36g氯化钠恰好达到饱和状态,即该温度时氯化钠的溶解度是36g.
故填:36g.
解:设AgNO3溶液中AgNO3的质量为x,则:
NaCl+AgNO3═AgCl↓+NaNO3
58.5 143.5
3.6g x
=
,
x=8.8g,
该硝酸银溶液中溶质的质量分数为:
×100%=8%.
答:AgNO3溶液中溶质质量分数约为8%.
故填:36g.
解:设AgNO3溶液中AgNO3的质量为x,则:
NaCl+AgNO3═AgCl↓+NaNO3
58.5 143.5
3.6g x
| 58.5 |
| 143.5 |
| 3.6g |
| x |
x=8.8g,
该硝酸银溶液中溶质的质量分数为:
| 8.8g |
| 105g |
答:AgNO3溶液中溶质质量分数约为8%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力.

练习册系列答案
相关题目
下列有关溶液的说法,正确的是( )
| A、凡是均一、透明、无色的液体都是溶液 | B、饱和溶液析出晶体后就变成了不饱和溶液 | C、某饱和溶液,当温度升高时(若溶液的质量不变),溶质的质量分数不变 | D、20℃时,氯化钠的溶解度为36克.在此温度下,将50克氯化钠固体溶解在50克水中所得溶液的溶质质量分数为50% |
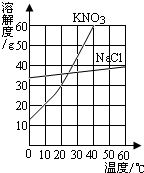 如图是硝酸钾和氯化钠在水中的溶解度曲线,请根据该曲线图回答下列问题:
如图是硝酸钾和氯化钠在水中的溶解度曲线,请根据该曲线图回答下列问题: 如图是硝酸钾和氯化钠在水中的溶解度曲线,请根据该曲线图回答下列问题:
如图是硝酸钾和氯化钠在水中的溶解度曲线,请根据该曲线图回答下列问题: