题目内容
【题目】如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示. 实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好. 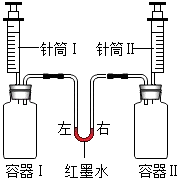
实验 | 容器I | 针筒I | 容器Ⅱ | 针筒Ⅱ | 红墨水 |
a | 10mL | NaCl | 10mL | 保持 | |
b | 二氧化碳 | 10mL | 二氧化碳 | 10mlL浓氢氧化钠溶液 | |
c | 1g锌 | 15mL盐酸 | 1g镁 | 15mL盐酸 |
(1)实验a中,容器Ⅰ内产生的现象是 . 红墨水液面位置发生变化的原因是(用化学方程式表示).
(2)实验b中,针筒Ⅰ、Ⅱ内盐酸足量且溶质质量分数相同,产生气泡更剧烈的是容器(填“Ⅰ”或“Ⅱ”).红墨水液面位置变化情况是 . 反应结束并恢复到原来的温度后,两边的红墨水保持相平.
【答案】
(1)澄清石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O
(2)Ⅱ;先是左高右低,最终红墨水左右两端液面保持相平
【解析】解:(1)实验a中,氢氧化钙溶液吸收二氧化碳比较彻底,而二氧化碳的溶解能力较差,因此红墨水液面位置保持左高右低; 二氧化碳能使澄清石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:澄清石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O.(2)实验b中,0.65g锌和足量的稀盐酸反应生成的氢气质量等于0.24g镁和足量的稀盐酸反应生成的氢气质量,因此最终红墨水左右两端液面保持相平;因为镁和稀盐酸反应比锌和稀盐酸反应剧烈,所以红墨水的位置先是左高右低.
故填:Ⅱ,先是左高右低,最终红墨水左右两端液面保持相平.
【考点精析】解答此题的关键在于理解二氧化碳的化学性质的相关知识,掌握化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应,以及对溶解时的吸热或放热现象的理解,了解溶解时放热、吸热现象<溶解吸热:如NH4NO3溶解;溶解放热:如NaOH溶解、浓H2SO4溶解;解没有明显热现象:如NaCl>.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案