��Ŀ����
����Ŀ��Ϊ�˲�ù�ҵ������̼���Ƶ����������������г�������NaCl����С��ͬѧ��Ƶ�ʵ��װ����ͼ�ף�ȷ��ȡһ�����Ĵ�����Ʒ���ӷ�Һ©���е���ϡ���ᣮ 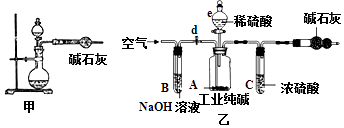
��1��ͼ����װ�÷����Ļ�ѧ����ʽΪ��
��2��С�����С����ʵ��װ�ûᵼ�½ϴ�����������ͼ�ҵ�װ�ã�����д��ͼ��װ�õ����ƣ�д�����㼴�ɣ�����
��3��С����ͼ��װ�ý���ʵ�鲽��Ϊ�� ��ȷ��ȡʢ�м�ʯ�ҵĸ���ܵ�����Ϊ158.0g����ȷ��ȡ11.0g������Ʒ��ȫ������A�У�����װȫ����Ӧװ�ò���������ԣ��ر�d����e��μ���ϡ���������ٲ�������Ϊֹ���۴�d�������������10min�� ���ٳƸ���ܵ�������Ϊ162.4g���ò�Ʒ��̼���Ƶ���������Ϊ���������ȷ��0.1%��
���𰸡�
��1��Na2CO3+H2SO4�TNa2SO4+H2O+CO2��
��2���ܹ���ֹˮ������ʵ��ĸ��ţ���ʹ��Ӧ���ɵĶ�����̼ȫ������ʯ������
��3��96.4%
���������⣺��1��ͼ���У�̼���ƺ�ϡ���ᷴӦ���������ơ�ˮ�Ͷ�����̼�������Ļ�ѧ����ʽΪ��Na2CO3+H2SO4�TNa2SO4+H2O+CO2���� ���Na2CO3+H2SO4�TNa2SO4+H2O+CO2������2��ͼ��װ�õ��ŵ��ǣ�������̼�е�ˮ�����ܱ�Cװ���е�Ũ�������գ��ܹ���ֹˮ������ʵ��ĸ��ţ�ʵ��������d�������������10min����ʹ��Ӧ���ɵĶ�����̼ȫ������ʯ�����գ�
����ܹ���ֹˮ������ʵ��ĸ��ţ���ʹ��Ӧ���ɵĶ�����̼ȫ������ʯ�����գ���3����̼��������Ϊx��
��Ӧ���ɶ�����̼����Ϊ��162.4g��158.0g=4.4g��
Na2CO3+H2SO4�TNa2SO4+H2O+ | CO2�� |
106 | 44 |
x | 4.4g |
![]() =
= ![]() ��
��
x=10.6g��
�ò�Ʒ��̼���Ƶ���������Ϊ�� ![]() ��100%=96.4%��
��100%=96.4%��
���96.4%��
�����㾫����������Ŀ����֪������������д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�����֪ʶ���Եõ�����Ĵ𰸣���Ҫ����ע�⣺a����ƽ b������ c�����ţ�

 ��������ϵ�д�
��������ϵ�д� ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�����Ŀ����ʵ����У���С����������ʵ�飺
ʵ���� | 1 | 2 | 3 | 4 |
ʵ����� |
|
|
|
|
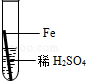
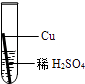
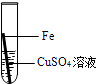
ʵ���ͬѧ�ǰ���ʦҪ��Һ������ָ���Ĵ��ձ��У�С�Ʋ�����ձ��еķ�Һ����������ͭ������п��������������Ӧ�ÿ��Դ�������������ͭ����˼�������������ͼ��ʾ��ʵ�飬���跨ʹ��Һ����������������ͬ��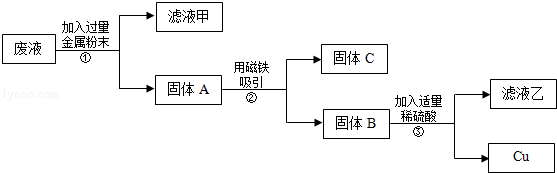
�����C�� �� �����۵������� �� ʵ�������ӵĹ���������ĩ�� ��