题目内容
【题目】蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收.丙氨酸(化学式为C3H7O2N)就是其中的一种.请回答下列问题;
(1)丙氨酸的相对分子质量为;丙氨酸中碳和氢元素的质量比为;
(2)丙氨酸中氮元素的质量分数为(计算结果精确到0.1%)
(3)89g丙氨酸所含的碳元素质量是多少g?(写出计算过程)
【答案】
(1)89;36:7
(2)15.7%
(3)解:89g丙氨酸所含的碳元素质量是89g× ![]() =36g
=36g
【解析】解:(1)丙酸铵的相对分子质量是12×3+1×7+16×2+14=89;丙氨酸中C、H素的质量比(12×3):(1×7)=36:7;故填:89;36:7;(2)丙氨酸中氮元素的质量分数为 ![]() ≈15.7%;故填:15.7%;
≈15.7%;故填:15.7%;

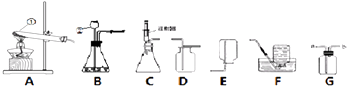
【题目】如图所示装置是初中化学的常见装置,用该装置可以完成不同的实验. 
(1)探究燃烧条件:若B处盛放木炭. Ⅰ.先在A处通入氮气一段时间后,在B处加热,B、C处没有明显变化;
Ⅱ.待B处冷却至室温,在A处通入氧气一段时间后,B、C处没有明显变化;
Ⅲ.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊.
② 能说明可燃物燃烧需要氧气的实验是(填实验序号).
②Ⅲ中石灰水变浑浊的反应方程式为 .
(2)模拟工业炼铁:若B处盛放赤铁矿粉末,利用一氧化碳进行还原. ①经检查装置气密性良好.为了防止爆炸,在用酒精喷灯给B处加热前应该先 , 点燃酒精喷灯一段时间后,B处可观察到的现象为 .
②某同学为了测定该赤铁矿石中氧化铁的质量分数,他称取了一定质量的赤铁矿石粉末,并通过正确的实验操作获得了如下数据:
反应前 | 完全反应后 | |
方法1 | 玻璃管和赤铁矿粉末的总质量为m1 | 玻璃管和固体物质的总质量为m2 |
方法2 | 试管和石灰水的总质量为m3 | 试管和试管中物质的总质量为m4 |
你认为他应该选择方法(填“1”或“2”)的实验数据来计算赤铁矿石中氧化铁质量分数,结果才更准确.
③用上述装置完成炼铁实验,有一明显不足,请改进