题目内容
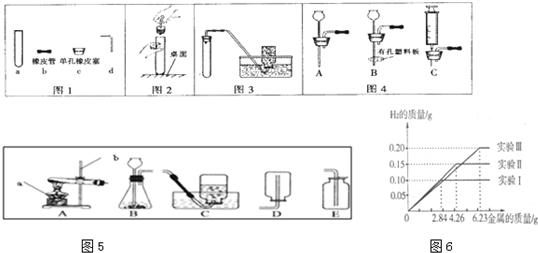
某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如图:试回答(计算结果精确到0.1%):
(1)写出实验中有关的化学方程式:______
(2)实验I中铁参加反应的质量为______.
(3)稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是多少?

【答案】分析:(1)根据铁和硫酸会发生置换反应进行分析;
(2)对比实验I、实验II,可得,实验I中2.84g钢样与稀硫酸完全反应,根据铁与硫酸反应生成硫酸亚铁和氢气的化学方程式,由反应放出氢气的质量可计算参加反应铁的质量;
(3)由实验I的数据可知,2.84g钢样完全反应放出氢气0.1g,同样组成的钢样4.26完全反应可放出氢气0.15g;而实验III取钢样6.23g时结果得到氢气只有0.2g,说明钢样未完全反应,则稀硫酸不足,稀硫酸完全反应;此时所得溶液为硫酸亚铁溶液,然后计算溶质的质量分数,硫酸亚铁质量要根据反应的化学方程式,由生成氢气质量计算;而反应后溶液质量可根据质量守恒进行计算.
解答:解:(1)铁和硫酸发生反应生成硫酸亚铁和氢气,故答案为:Fe+H2SO4═FeSO4+H2↑;
(2)设实验I中参加反应的铁的质量为x,
Fe+H2SO4═FeSO4+H2↑
56 2
x 0.1g
 =
=
x=2.8g
故答案为:2.8g
(3)由表中数据分析,实验Ⅲ中100g稀硫酸完全反应.
设实验Ⅲ生成硫酸亚铁的质量为x,消耗铁的质量为y.
Fe+H2SO4═FeSO4+H2↑
56 152 2
y x 0.2g
 =
= ,
, =
= ,
,
x=15.2g y=5.6g
所得溶液中溶质的质量分数为 ×100%=14.4%.
×100%=14.4%.
答:反应后溶液中溶质的质量分数是14.4%.
点评:根据质量守恒定律,稀硫酸完全反应的实验III所得溶液质量=稀硫酸质量+钢样中参加反应铁的质量-生成氢气的质量.
(2)对比实验I、实验II,可得,实验I中2.84g钢样与稀硫酸完全反应,根据铁与硫酸反应生成硫酸亚铁和氢气的化学方程式,由反应放出氢气的质量可计算参加反应铁的质量;
(3)由实验I的数据可知,2.84g钢样完全反应放出氢气0.1g,同样组成的钢样4.26完全反应可放出氢气0.15g;而实验III取钢样6.23g时结果得到氢气只有0.2g,说明钢样未完全反应,则稀硫酸不足,稀硫酸完全反应;此时所得溶液为硫酸亚铁溶液,然后计算溶质的质量分数,硫酸亚铁质量要根据反应的化学方程式,由生成氢气质量计算;而反应后溶液质量可根据质量守恒进行计算.
解答:解:(1)铁和硫酸发生反应生成硫酸亚铁和氢气,故答案为:Fe+H2SO4═FeSO4+H2↑;
(2)设实验I中参加反应的铁的质量为x,
Fe+H2SO4═FeSO4+H2↑
56 2
x 0.1g
 =
=
x=2.8g
故答案为:2.8g
(3)由表中数据分析,实验Ⅲ中100g稀硫酸完全反应.
设实验Ⅲ生成硫酸亚铁的质量为x,消耗铁的质量为y.
Fe+H2SO4═FeSO4+H2↑
56 152 2
y x 0.2g
 =
= ,
, =
= ,
,x=15.2g y=5.6g
所得溶液中溶质的质量分数为
 ×100%=14.4%.
×100%=14.4%. 答:反应后溶液中溶质的质量分数是14.4%.
点评:根据质量守恒定律,稀硫酸完全反应的实验III所得溶液质量=稀硫酸质量+钢样中参加反应铁的质量-生成氢气的质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如下图象:
某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如下图象: 某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.28g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验Ⅰ、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如下图象:
某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.28g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验Ⅰ、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如下图象: 某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.24g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如图象:
某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.24g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如图象: (2010?怀柔区一模)某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制成如下图象:
(2010?怀柔区一模)某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制成如下图象: