题目内容
常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉.
脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 (红褐色固体)
(1)Fe(OH)2读作________.
(2)某同学用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行两个实验:
实验Ⅰ:
请回答:
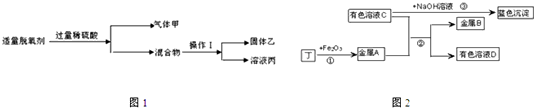
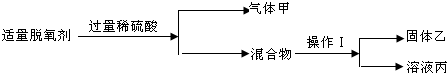
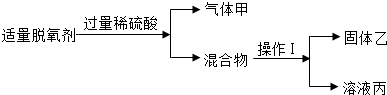
如图1,①操作Ⅰ的名称是________;
②溶液丙中含有的金属阳离子是________(写微粒符号)
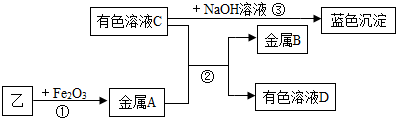
实验Ⅱ:将乙洗涤烘干后,二氧化碳通过灼热的乙生成丁.进行如图2实验,物质之间的转化关系如图(部分产物略去).
①金属A与B的活动性:A________B(填“>”“<”或“﹦”);
②区别有色溶液C与有色溶液D的方法是________;
③反应①的化学方程式为:________;
④向溶液C中加入BaCl2溶液,有白色沉淀产生.其化学方程式为________.
解:(1)铁元素显+2价时读作亚铁,故Fe(OH)2读作氢氧化亚铁;
(2)实验Ⅰ:
①将固体和液体分离的操作叫做过滤,故答案为:过滤.
②溶液丙中含有的溶质有:反应生成的硫酸亚铁,原来的氯化钠,还有没有反应的硫酸.故填:Fe2+、Na+.
实验Ⅱ:
①金属A能将金属B从它的盐溶液中置换出来,故答案:活动性A>B.
②区别溶液C与溶液D物质的方法是:观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液.
③一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO 2Fe+3CO2;
2Fe+3CO2;
④硫酸铜和氯化钡反应能生成硫酸钡沉淀和氯化铜,反应的化学方程式为:CuSO4+BaCl2=BaSO4↓+CuCl2.
故答案为:(1)氢氧化亚铁
(2)实验Ⅰ:①过滤;②Fe2+、Na+.
实验Ⅱ:①>
②观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液(或分别取两种溶液,分别加入NaOH溶液,最后有红褐色沉淀的是FeSO4溶液,有蓝色沉淀的是CuSO4溶液);③Fe2O3+3CO 2Fe+3CO2; ④CuSO4+BaCl2═BaSO4↓+CuCl2;
2Fe+3CO2; ④CuSO4+BaCl2═BaSO4↓+CuCl2;
分析:(1)根据物质的化学式的读法,从后向前读作某化某,可以读出物质的名称;
(2)实验Ⅰ:
过滤可以把不溶于水的物质除去,活性炭具有吸附性,常常用作吸附剂;
根据反应过程可以判断溶液中的溶质.
实验Ⅱ:
根据活泼性强的金属可以把不如他活泼的金属从它的盐溶液中置换出来进行分析;
可以通过颜色来判断具体的物质;
根据反应物和生成物及其质量守恒定律可以书写化学方程式.
点评:本题主要考查实验探究方面的知识,解答时要掌握物质之间相互作用时的反应情况,特别是要能够根据物质的性质方面的知识来判断具体的物质,并且能够根据质量守恒定律的内容正确的书写反应的化学方程式.
(2)实验Ⅰ:
①将固体和液体分离的操作叫做过滤,故答案为:过滤.
②溶液丙中含有的溶质有:反应生成的硫酸亚铁,原来的氯化钠,还有没有反应的硫酸.故填:Fe2+、Na+.
实验Ⅱ:
①金属A能将金属B从它的盐溶液中置换出来,故答案:活动性A>B.
②区别溶液C与溶液D物质的方法是:观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液.
③一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO
 2Fe+3CO2;
2Fe+3CO2;④硫酸铜和氯化钡反应能生成硫酸钡沉淀和氯化铜,反应的化学方程式为:CuSO4+BaCl2=BaSO4↓+CuCl2.
故答案为:(1)氢氧化亚铁
(2)实验Ⅰ:①过滤;②Fe2+、Na+.
实验Ⅱ:①>
②观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液(或分别取两种溶液,分别加入NaOH溶液,最后有红褐色沉淀的是FeSO4溶液,有蓝色沉淀的是CuSO4溶液);③Fe2O3+3CO
 2Fe+3CO2; ④CuSO4+BaCl2═BaSO4↓+CuCl2;
2Fe+3CO2; ④CuSO4+BaCl2═BaSO4↓+CuCl2;分析:(1)根据物质的化学式的读法,从后向前读作某化某,可以读出物质的名称;
(2)实验Ⅰ:
过滤可以把不溶于水的物质除去,活性炭具有吸附性,常常用作吸附剂;
根据反应过程可以判断溶液中的溶质.
实验Ⅱ:
根据活泼性强的金属可以把不如他活泼的金属从它的盐溶液中置换出来进行分析;
可以通过颜色来判断具体的物质;
根据反应物和生成物及其质量守恒定律可以书写化学方程式.
点评:本题主要考查实验探究方面的知识,解答时要掌握物质之间相互作用时的反应情况,特别是要能够根据物质的性质方面的知识来判断具体的物质,并且能够根据质量守恒定律的内容正确的书写反应的化学方程式.

练习册系列答案
相关题目

 (2012?通州区二模)人类生活离不开金属.
(2012?通州区二模)人类生活离不开金属.