题目内容
化学实验是我们进一步认识物质及其变化的重要方式.请根据如图回答问题
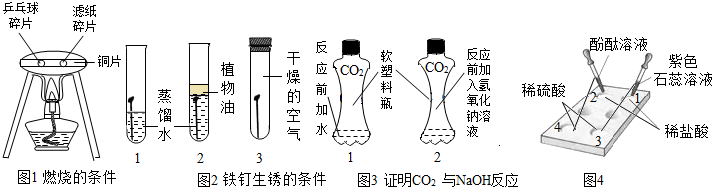 (1)通过实验,可以说明燃烧的条件之一是 ,实验中使用了铜片,这是利用了铜的 性.(填一条物理性质)
(1)通过实验,可以说明燃烧的条件之一是 ,实验中使用了铜片,这是利用了铜的 性.(填一条物理性质)
(2)对于图2实验,一段时间后,③铁钉没有锈蚀,而①铁钉锈蚀,通过①②实验对比,说明铁钉锈蚀的条件之一是 ,用盐酸除铁锈的化学方程式是 .
(3)图3实验是利用体积相同并充满了CO2软塑料瓶,等量的水和(瓶①)和NaOH溶液(瓶②)进行实验,根据 的程度证明CO2 与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为
(4)图4实验观察到1、3孔中的现象是 ,该实验目的是探究 .
 (1)通过实验,可以说明燃烧的条件之一是
(1)通过实验,可以说明燃烧的条件之一是(2)对于图2实验,一段时间后,③铁钉没有锈蚀,而①铁钉锈蚀,通过①②实验对比,说明铁钉锈蚀的条件之一是
(3)图3实验是利用体积相同并充满了CO2软塑料瓶,等量的水和(瓶①)和NaOH溶液(瓶②)进行实验,根据
(4)图4实验观察到1、3孔中的现象是
考点:燃烧与燃烧的条件,金属锈蚀的条件及其防护,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:实验性简答题
分析:(1)根据燃烧的条件以及铜具有良好的导热性进行解答;
(2)根据铁生锈的主要条件是铁与水和空气直接接触进行解答;
(3)根据二氧化碳和NaOH溶液反应生成碳酸钠和水进行解答;
(4)根据石蕊遇酸变红,酚酞遇酸不变色结合实验的相同点碱性对比分析;
(2)根据铁生锈的主要条件是铁与水和空气直接接触进行解答;
(3)根据二氧化碳和NaOH溶液反应生成碳酸钠和水进行解答;
(4)根据石蕊遇酸变红,酚酞遇酸不变色结合实验的相同点碱性对比分析;
解答:解:
(1)燃烧的条件:物质具有可燃性、与氧气接触、温度达到可燃物的着火点,实验A中滤纸碎片和乒乓球碎片都与氧气接触,在加热过程中,利用铜片的导热性,在中间加热,能够提供均匀的热量,由于乒乓球碎片的着火点较低,首先燃烧起来,说明燃烧需要温度达到可燃物的着火点;
故填:温度达到可燃物的着火点;导热;
(2)对于实验B,一段时间观察试管①中的铁钉明显锈蚀,①试管中即提供了空气,也提供了水,②只与水接触没有生锈,由此得出:铁生锈的条件除了水,还必须与氧气接触;盐酸和氧化铁反应产生氯化铁和水,故填:铁钉与氧气接触;Fe2O3+6HCl=2FeCl3+3H2O;
(3)实验C是根据塑料瓶变瘪的程度证明CO2 与NaOH溶液中的溶质确实发生了反应,(瓶①)的作用是对比,证明不是因为二氧化碳溶于水是瓶变瘪,二氧化碳和NaOH溶液反应生成碳酸钠和水,故反应的化学方程式为2NaOH+CO2═Na2CO3+H2O;
(4)石蕊试液遇酸变红色,因此1、3孔中会观察到稀盐酸、稀硫酸使石蕊试液变成红色,而2、4孔的酚酞试液与盐酸、硫酸不变色,因此通过对比可以探究酸雨指示剂的作用;故答案为:溶液变红,酸与指示剂作用.
(1)燃烧的条件:物质具有可燃性、与氧气接触、温度达到可燃物的着火点,实验A中滤纸碎片和乒乓球碎片都与氧气接触,在加热过程中,利用铜片的导热性,在中间加热,能够提供均匀的热量,由于乒乓球碎片的着火点较低,首先燃烧起来,说明燃烧需要温度达到可燃物的着火点;
故填:温度达到可燃物的着火点;导热;
(2)对于实验B,一段时间观察试管①中的铁钉明显锈蚀,①试管中即提供了空气,也提供了水,②只与水接触没有生锈,由此得出:铁生锈的条件除了水,还必须与氧气接触;盐酸和氧化铁反应产生氯化铁和水,故填:铁钉与氧气接触;Fe2O3+6HCl=2FeCl3+3H2O;
(3)实验C是根据塑料瓶变瘪的程度证明CO2 与NaOH溶液中的溶质确实发生了反应,(瓶①)的作用是对比,证明不是因为二氧化碳溶于水是瓶变瘪,二氧化碳和NaOH溶液反应生成碳酸钠和水,故反应的化学方程式为2NaOH+CO2═Na2CO3+H2O;
(4)石蕊试液遇酸变红色,因此1、3孔中会观察到稀盐酸、稀硫酸使石蕊试液变成红色,而2、4孔的酚酞试液与盐酸、硫酸不变色,因此通过对比可以探究酸雨指示剂的作用;故答案为:溶液变红,酸与指示剂作用.
点评:此题是一道综合性的实验设计题,解题的关键是掌握燃烧的条件、铁生锈的条件、二氧化碳的性质、酸碱指示剂的性质并进行知识的大胆迁移,只有这样才能顺利解题.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案
相关题目
“低碳生活”是指减少能源消耗,节约资源,从而减少二氧化碳排放的生活方式.下列不符合“低碳生活”的做法是( )
| A、出门随手关灯 |
| B、草稿纸双面使用 |
| C、骑自行车代替乘公交车出行 |
| D、废旧书籍和废弃塑料做焚烧处理 |
 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.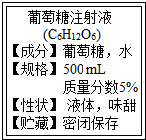 如图是某输液瓶标签上的部分内容,请回答:
如图是某输液瓶标签上的部分内容,请回答: