题目内容
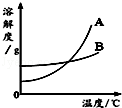
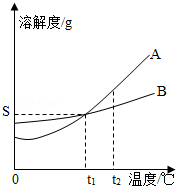
下图是A、B、C三种固体物质的溶解度曲线。下列分析不正确的是
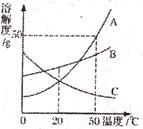
A.50℃时,三种物质的溶解度由大到小的顺序是A>B>C
B.50℃时,把50 g A放入50 g水中能形成75 g A的饱和溶液
C.将C的饱和溶液变为不饱和溶液,可采用降温的方法
D.分别将三种物质的饱和溶液从50℃将至20℃时,所得溶液溶质质量分数大小关系是B>C=A

A.50℃时,三种物质的溶解度由大到小的顺序是A>B>C
B.50℃时,把50 g A放入50 g水中能形成75 g A的饱和溶液
C.将C的饱和溶液变为不饱和溶液,可采用降温的方法
D.分别将三种物质的饱和溶液从50℃将至20℃时,所得溶液溶质质量分数大小关系是B>C=A
D
比较饱和溶液的溶质质量分数只需比较相应温度下的溶解度,溶解度越大,溶质质量分数越大。由于A、B的溶解度都随温度升高而增大,所以这两种物质的饱和溶液降温刊,溶液仍然是饱和溶液,但由于有溶质析出,所以溶液的溶质质量分数减小,所以降温后B的溶质质量分数大于A,由于C的溶解度随温度升高而减小,所以饱和溶液降温后变为不饱和溶液,其溶质质量分数不变,由于20℃时A的溶解度大于50℃C的溶解度,所以降温后A溶液的溶质质量分数大于C溶液的溶质质量分数,即降温后,溶液的溶质质量分数由大到小的顺序为B>A>C。

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目