题目内容
【题目】一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学,合成气可通过天然气的重整得到,如CH4+H2O═CO+3H2。合成气可制二甲醚,二甲醚被称为21世纪的新型燃料。合成气还可用于冶炼金属。请你仔细阅读合成气冶炼粗铜和制取二甲醚的部分生产流程,回答下列问题:

(1)铜绿[化学式为Cu2(OH)2CO3]中碳元素、氧元素的质量比为 。合成气在与黑色固体冶炼粗铜的生产过程中发生的反应方程式为 (写出其中一个反应)。
(2)二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制的。用合成气制二甲醚时,还产生了一种常温为液态的氧化物,写出该反应的化学方程式: 。
(3)上述生产流程的突出优点是 。
(4)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质。仅用合成气为原料不可能得到的物质是 (填字母序号)。
A.草酸(H2C2O4) B.甲醇(CH3OH) C.尿素[CO(NH2)2]
【答案】(1)C:O=12:80=3:20 方程式略。
(2)2CO+4H2═CH3OCH3+H2O
(3)重复利用尾气中的二氧化碳气体,既防止温室效应,又节约原料
(4)AC(多选、少选均不得分)
【解析】本题考查的是物质的相互转化和制备、元素质量比的计算、质量守恒定律及其应用、以及正确书写化学方程式。
![]() (1)铜绿[化学式为Cu2(OH)2CO3]中碳元素、氧元素的质量比为 12:16×5=3:20。合成气一氧化碳与氢气具有还原性,铜绿分解生成的黑色固体是氧化铜,一氧化碳与氧化铜反应生成铜和二氧化碳.反应方程式为
(1)铜绿[化学式为Cu2(OH)2CO3]中碳元素、氧元素的质量比为 12:16×5=3:20。合成气一氧化碳与氢气具有还原性,铜绿分解生成的黑色固体是氧化铜,一氧化碳与氧化铜反应生成铜和二氧化碳.反应方程式为
(2)由题意可知合成气(CO和H2)在一定的条件下能生成二甲醚(CH3OCH3)和水,写出该反应的化方程式:2CO+4H2═CH3OCH3+H2O
(3)上述生产流程中铜绿分解生成二氧化碳,一氧化碳还原氧化铜也生成二氧化碳,二氧化碳水和甲烷能重整生成一氧化碳和氢气,因此重复利用尾气中的二氧化碳气体,既防止温室效应,又节约原料。
(4)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质.根据反应前后元素种类不变,原子个数不变,可知反应前后碳原子与氧原子个数比一定是1:1,而A中碳原子与氧原子个数比是1:2,C中生成物中有氮元素(反应前后元素种类不变),不可能得到。故选 AC

 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案【题目】运用溶解度表与溶解度曲线回答下列问题:
温度/℃ | 10 | 30 | 50 | 60 | |
溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
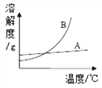
(1)氯化钠的溶解度曲线是______ (填“A”或“B”)。
(2)60℃时,100g水中加入90g硝酸钾,充分溶解,所得溶液是____(填“饱和”或“不饱和”)溶液。当60℃的该溶液降温到10℃时,析出晶体的质量为___________ g。
(3)将30℃的KNO3饱和溶液升温到50℃(不考虑水分蒸发),其溶质的质量分数_______(填“变大”、“变小”或“不变”)。