题目内容
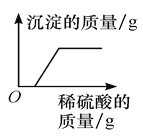
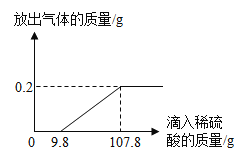
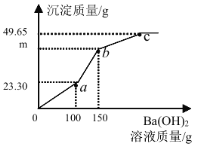
【题目】烧杯中盛有 CuSO4 和 HCl 的混合溶液 100.0g,向其中逐滴滴加 Ba(OH)2 溶液,产生沉淀的质量与滴加的溶液质量关系如图所示。下列说法正确的是
A.a 点对应溶液中有 1 种溶质
B.b~c 段发生 2 个反应
C.HCl 在原溶液中的溶质质量分数约为 14.6%
D.m=39.85
【答案】D
【解析】
向CuSO4 和 HCl 混合溶液中逐滴滴加 Ba(OH)2 溶液的过程中,钡离子先和硫酸根离子反应生成白色的硫酸钡沉淀;氢氧根先和氢离子反应生成水,等氢离子反应完全后再和铜离子反应生成氢氧化铜沉淀;因此o-a段生成的是硫酸钡沉淀,a-b段生成的是硫酸钡和氢氧化铜沉淀,b-c段生成的是氢氧化沉铜淀。
A、a点对应溶液中有氯化铜、硫酸铜2种溶质,故选项说法错误。
B、b~c段只发生氢氧化钡和氯化铜1个反应,故选项说法错误。
C、设盐酸中溶质HCl的质量分数为x,氢氧化钡的质量分数为y。由反应物与生成物的配比关系可得。
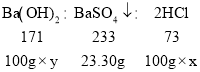
![]()
解得:x=7.3%,y=17.1%。故选项说法错误。
D、设硫酸钡的质量为a,氢氧化铜的质量为b。
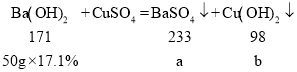
![]()
解得:a=11.65g;b=4.9g。
所以m=23.3g+11.65g+4.9=39.85g,故选项说法正确。
故选:D。

练习册系列答案
相关题目