题目内容
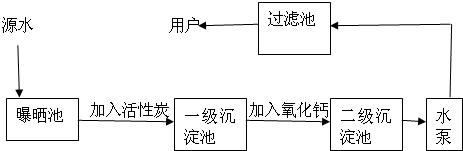
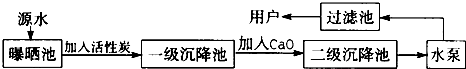
25、某自来水厂用源水处理成自来水的流程如下:
(1)加入活性炭的作用是
(2)实验室中,静置、吸附、过滤、蒸馏等操作中可以降低水硬度的是
(3)自来水厂净水过程中需加消毒剂.二氧化氯(ClO2)是新一代饮用水的消毒剂,其中氯元素的化合价为
(4)若该地区源水中含有较多的MgCl2,请写出在源水处理流程中加入CaO时有关化学方程式:①

(1)加入活性炭的作用是
吸附水中的色素和异味
;若没有活性炭,可以加入木炭
来净水;(2)实验室中,静置、吸附、过滤、蒸馏等操作中可以降低水硬度的是
蒸馏
;若在实验室进行该操作,需要用到的玻璃仪器除蒸馏烧瓶、冷凝管、尾接管、温度计、锥形瓶、外,还有酒精灯
.(3)自来水厂净水过程中需加消毒剂.二氧化氯(ClO2)是新一代饮用水的消毒剂,其中氯元素的化合价为
+4
;(4)若该地区源水中含有较多的MgCl2,请写出在源水处理流程中加入CaO时有关化学方程式:①
CaO+H2O=Ca(OH)2
;②MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2
.分析:(1)活性炭、木炭等物质具有吸附作用,能够吸附水中的色素和异味.
(2)加热时,水中的钙离子和镁离子能够以沉淀的形式从水中析出;加热时应该用酒精灯.
(3)在化合物中元素化合价的代数和为零.
(4)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
(2)加热时,水中的钙离子和镁离子能够以沉淀的形式从水中析出;加热时应该用酒精灯.
(3)在化合物中元素化合价的代数和为零.
(4)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
解答:解:(1)加入活性炭的作用是吸附水中的色素和异味.故填:吸附水中的色素和异味.
若没有活性炭,可以加入木炭来净水.故填:木炭.
(2)实验室中,静置、吸附、过滤、蒸馏等操作中可以降低水硬度的是蒸馏.故填:蒸馏.
若在实验室进行该操作,需要用到的玻璃仪器除蒸馏烧瓶、冷凝管、尾接管、温度计、锥形瓶外,还有酒精灯.故填:酒精灯.
在二氧化氯中,氧元素的化合价是-2价,可以求出氯元素的化合价为+4价.故填:+4.
(4)氧化钙和水反应能生成氢氧化钙,氢氧化钙和氯化镁反应能生成氢氧化镁沉淀和氯化钙,反应的化学方程式分别为:
CaO+H2O=Ca(OH)2 ;Mg(OH)2↓+CaCl2.
若没有活性炭,可以加入木炭来净水.故填:木炭.
(2)实验室中,静置、吸附、过滤、蒸馏等操作中可以降低水硬度的是蒸馏.故填:蒸馏.
若在实验室进行该操作,需要用到的玻璃仪器除蒸馏烧瓶、冷凝管、尾接管、温度计、锥形瓶外,还有酒精灯.故填:酒精灯.
在二氧化氯中,氧元素的化合价是-2价,可以求出氯元素的化合价为+4价.故填:+4.
(4)氧化钙和水反应能生成氢氧化钙,氢氧化钙和氯化镁反应能生成氢氧化镁沉淀和氯化钙,反应的化学方程式分别为:
CaO+H2O=Ca(OH)2 ;Mg(OH)2↓+CaCl2.
点评:本题主要考查净化水方面的知识,书写化学方程式时要正确书写反应物和生成物的化学式,要遵循质量守恒定律.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目