题目内容
【题目】实验室有一瓶标签模糊的烧碱溶液,小杰设计实验测定了其溶质质量分数.请根据如图所示的实验过程和提供的数据进行分析和计算.(注:滴入酚酞试液的质量忽略不计)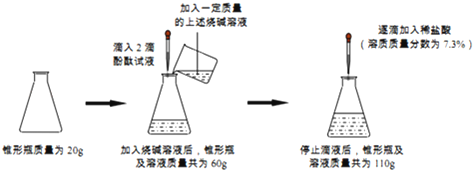
(1)将稀盐酸逐滴滴入锥形瓶的过程中,应边滴加边摇动锥形瓶,当观察到溶液颜色恰好时,停止滴液,反应所消耗稀盐酸的质量为g.
(2)通过计算确定该瓶烧碱溶液的溶质质量分数.(写出计算步骤)
(3)问题讨论:小红做同样的实验得到的结果比小杰得到的结果偏小,从实验操作的角度分析产生这种误差的原因可能是(填写一条即可)
【答案】
(1)无色;50
(2)
所取烧碱溶液的质量为:60g﹣20g=40g.
设烧碱溶液的溶质质量为x,
NaOH+HCl=NaCl+H2O
40 36.5
x 50g×7.3%
![]()
x=0.4g
答:该瓶烧碱溶液的溶质质量分数=![]()
![]() =10%。
=10%。
(3)滴加的稀硫酸过量
【解析】解:(1)将稀盐酸逐滴滴入锥形瓶的过程中,应边滴加边摇动锥形瓶,当观察到溶液颜色恰好无色时,停止滴液,反应所消耗稀盐酸的质量为110g﹣60g=50g;
(2)所取烧碱溶液的质量为:60g﹣20g=40g.
设烧碱溶液的溶质质量为x,
NaOH+HCl=NaCl+H2O
40 36.5
x 50g×7.3%![]()
x=0.4g
答:该瓶烧碱溶液的溶质质量分数=![]()
![]() =10%。
=10%。
3)小红做同样的实验得到的结果比小杰得到的结果偏小,从实验操作的角度分析产生这种误差的原因可能是滴加的稀硫酸过量.
答案:(1)无色;50;(2)该瓶烧碱溶液的溶质质量分数为10%;(3)滴加的稀硫酸过量.
(1)根据酚酞溶液遇碱性溶液呈红色,遇中性溶液为无色解答;根据质量守恒定律反应所消耗的稀盐酸质量=反应后所得物质的总质量﹣反应前所有物质的总质量;(2)根据化学方程式结合氢氧化钠的质量可以计算出硫酸的质量进而就算出其溶质的质量分数;(3)根据所用盐酸过量,故计算出的结果要偏大.本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.解题的关键是分析反应物与生成物之间的质量关系.