题目内容
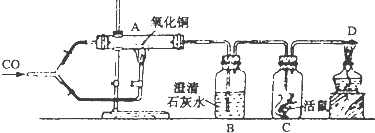
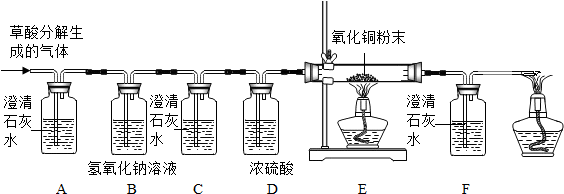
某化学课外兴趣小组通过查阅资料知道过氧化钠(Na2O2)能与水反应生成氢氧化钠和氧气,于是他们做了以下探究实验.
实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来.请你对脱脂棉燃烧的原因进行分析________.
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了.
[提出问题]溶液为什么先变红,过了一会,红色又褪去了呢?
[猜想]甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故.乙同学认为甲同学的猜想不正确,理由是________.
[查阅资料]①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色.
[猜想]通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因进行了猜想.
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓.
[实验探究]请你将下列实验方案填写完整.

答案:
解析:
解析:
|
实验1:反应中产生氧气和放出热量,使脱脂棉达到燃烧的条件(2分) 实验2:氢氧化钠溶液与二氧化碳反应后生成的碳酸钠溶液也显碱性,也能使酚酞试液变为红色
|

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
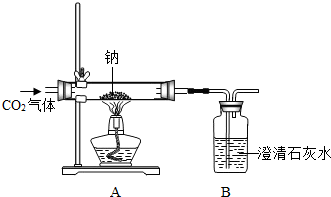
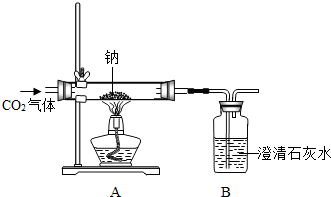
某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.
资料卡:
(1)K、Ca、Na等活泼金属的氧化物均可与水反应生成对应的碱;
(2)钠为银白色金属,过氧化钠为淡黄色固体.
(一)提出问题:白色固体含有什么物质?
(二)猜想与假设:
假设1:白色固体含有 ;
假设2:白色固体含有Na2O;
(三)实验设计:
(四)反思提高:
Na在CO2中燃烧存在多个反应、生成多种物质.请你写出其中生成物仅为一种白色固体与一种黑色固体的反应的化学方程式: .

资料卡:
(1)K、Ca、Na等活泼金属的氧化物均可与水反应生成对应的碱;
(2)钠为银白色金属,过氧化钠为淡黄色固体.
(一)提出问题:白色固体含有什么物质?
(二)猜想与假设:
假设1:白色固体含有
假设2:白色固体含有Na2O;
(三)实验设计:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量白色固体放入足量水中 | 白色固体完全溶解 | |
| ②取①中少量溶液,加入 |
产生大量气泡 | 假设1成立 |
| ③另取①中少量溶液, |
假设2成立 |
Na在CO2中燃烧存在多个反应、生成多种物质.请你写出其中生成物仅为一种白色固体与一种黑色固体的反应的化学方程式:

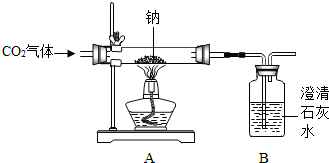 (2013?苍梧县二模)某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如右图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.
(2013?苍梧县二模)某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如右图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.