题目内容
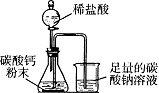
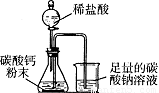
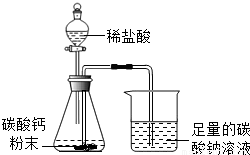
如图所示,用分液漏斗向盛有碳酸钙粉末的锥形瓶内加入过量的稀盐酸至图中位置,关闭分液漏斗的活塞.(装置的气密性良好)整个实验过程中你能观察到的现象有: ;请你解释原因: .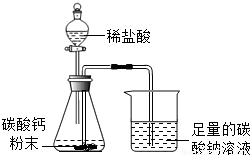
【答案】分析:根据碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,产生的二氧化碳不能排出,压强越来越大,把左侧的液体压入右侧,再根据物质之间的反应说出现象即可.
解答:解:碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,产生的二氧化碳不能排出,压强越来越大,把左侧的液体压入右侧烧杯中,进来的过量的盐酸会与碳酸钠反应生成氯化钠、水、二氧化碳,所以开始右侧有气泡产生,碳酸钙与盐酸反应生成的氯化钙也会进入烧杯中,氯化钙与碳酸钠反应生成碳酸钙白色沉淀和氯化钠,所以会产生白色沉淀.
故答案为:(1)锥形瓶内白色固体逐渐减少到消失,产生气泡,锥形瓶中的液体沿导管进入右侧烧杯内;烧杯内的液体中先产生气泡,后产生白色沉淀.
(2)碳酸钙与稀盐酸反应生成二氧化碳、氯化钙和水,使锥形瓶内气体量增加,气压增大,大于外压,在气压差的作用下,瓶内液体进入烧杯中;碳酸钠先与剩余的盐酸反应生成二氧化碳气体,后与氯化钙反应生成碳酸钙白色不溶于水的固体.
点评:解答本题关键是要知道产生的二氧化碳排不出来就会产生压力差,将左侧中的液体压入右侧.
解答:解:碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,产生的二氧化碳不能排出,压强越来越大,把左侧的液体压入右侧烧杯中,进来的过量的盐酸会与碳酸钠反应生成氯化钠、水、二氧化碳,所以开始右侧有气泡产生,碳酸钙与盐酸反应生成的氯化钙也会进入烧杯中,氯化钙与碳酸钠反应生成碳酸钙白色沉淀和氯化钠,所以会产生白色沉淀.
故答案为:(1)锥形瓶内白色固体逐渐减少到消失,产生气泡,锥形瓶中的液体沿导管进入右侧烧杯内;烧杯内的液体中先产生气泡,后产生白色沉淀.
(2)碳酸钙与稀盐酸反应生成二氧化碳、氯化钙和水,使锥形瓶内气体量增加,气压增大,大于外压,在气压差的作用下,瓶内液体进入烧杯中;碳酸钠先与剩余的盐酸反应生成二氧化碳气体,后与氯化钙反应生成碳酸钙白色不溶于水的固体.
点评:解答本题关键是要知道产生的二氧化碳排不出来就会产生压力差,将左侧中的液体压入右侧.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
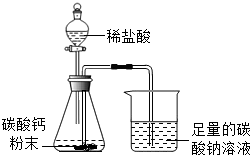 如图所示,用分液漏斗向盛有碳酸钙粉末的锥形瓶内加入过量的稀盐酸至图中位置,关闭分液漏斗的活塞.(装置的气密性良好)整个实验过程中你能观察到的现象有:
如图所示,用分液漏斗向盛有碳酸钙粉末的锥形瓶内加入过量的稀盐酸至图中位置,关闭分液漏斗的活塞.(装置的气密性良好)整个实验过程中你能观察到的现象有: