��Ŀ����
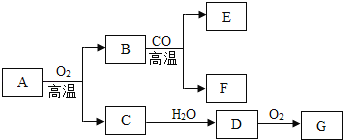
����Ŀ��A��G��������֮�������ͼ��ʾת����ϵ����֪��A��һ�ֺ����Ŀ�ʯ����Ҫ�ɷ֣�������Ԫ�أ������н�����ǽ���Ԫ�ص�ԭ�Ӹ�����Ϊ1��2��B�Ǻ���ɫ���壻C���д̼�����ζ����ɫ���壬�����γ��������Ҫ����֮һ��F������G��ϡ��Һ���������壬�������������ڻ�������������ȼ�ϡ���ش��������⣺
��1��A�Ļ�ѧʽΪ_____����֪Aת��ΪBʱ����Ԫ�صĻ��ϼ����ߣ���A�зǽ���Ԫ�صĻ��ϼ���_____��
��2��B��CO��Ӧ�Ļ�ѧ����ʽ��_____��
��3��B��G��ϡ��Һ��Ӧ�Ļ�ѧ����ʽ��_____��
���𰸡�FeS2 ��1 Fe2O3+3CO![]() 2Fe+3CO2 Fe2O3+3H2SO4��Fe2��SO4��3+3H2O
2Fe+3CO2 Fe2O3+3H2SO4��Fe2��SO4��3+3H2O
��������
A��һ�ֺ����Ŀ�ʯ����Ҫ�ɷ֣�������Ԫ�أ������н�����ǽ���Ԫ�ص�ԭ�Ӹ�����Ϊ1��2����A����Ϊ����������B�Ǻ���ɫ���壬��B��������������C���д̼�����ζ����ɫ���壬�����γ��������Ҫ����֮һ����C�Ƕ���������ˮ��Ӧ���ɵ�D�������ᣬ�������ܱ�����Ϊ���ᣬ��G�����ᣬ�������ܱ�һ����̼��ԭΪ��ͬʱ���ɶ�����̼�������ͼ���ƶϺ�����
�ɷ�����֪��1��A�Ƕ���������B����������Aת��ΪBʱ����Ԫ�صĻ��ϼ����ߣ�����A����Ԫ����+2�ۣ�����Ԫ�صĻ��ϼ�Ϊ��1��
��2��һ����̼�������������·�Ӧ�������Ͷ�����̼����Ӧ�Ļ�ѧ����ʽ�ǣ�Fe2O3+3CO![]() 2Fe+3CO2��
2Fe+3CO2��
��3���������������ᷴӦ������������ˮ����Ӧ�Ļ�ѧ����ʽ�ǣ�Fe2O3+3H2SO4��Fe2��SO4��3+3H2O��