��Ŀ����
����Ŀ���ҹ������߳���3.2��ǧ�ף�����ר����������Ա������������Դ�ḻ������ǰ��ʮ��Զ��
��1 ���ҹ����������3ǧ����֣��������һλ��Ŀǰ�Ӻ�ˮ����ȡʳ�εķ�����ҪΪ��
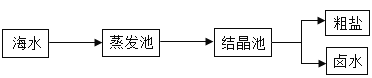
һ�������ĺ�ˮ��ͨ����ˮ�����뵽�����أ���û������ᾧ��֮ǰ�����������У����������Ȼ��Ƶ������� ������������䡱��|��С������
��2���������㷺Ӧ�����������������ҵ����±ˮ����ȡþ�Ĺ�����ͼ��ʾ��
![]()
������ת�������У��ٴ��������ķ�Ӧ���� ��Ӧ����к͡������ֽ⡰�������������ϡ����ֽ⡰֮һ��
��3����ˮ�г����̺���������Ԫ�غ�þԪ���⣬�����д����ļ�Ԫ�أ�KCl��KNO3���ܽ��������ͼ��ʾ���Իش��������⣺

��t1��ʱ��KCl������Һ�����ʵ��������� KNO3������Һ��������������������ڡ���С�ڡ������ڡ�֮һ��
��t2��ʱKCl��KNO3���ܽ�����߽���һ�㣬�õ��ʾ������Ϊ ��
����KNO3�л�������KCl���ɲ��� �ķ����ᴿKNO3��
����֪20��ʱ��KNO3���ܽ��Ϊ31.6g��80��ʱ��KNO3���ܽ��Ϊ169g����20��ʱ����ʢ��100gˮ���ձ��м���40gKNO3������ܽ⣬�õ����¶�ʱKNO3�ģ�����͡��������͡�֮һ����Һ����ʹ�ձ������ʻ���������40�棬�ڸ��¶��£����������Һ���������ܼ�������֮��Ϊ ������������ȣ���
���𰸡���1�������䣻��2�����ֽ⣻��3���ٴ��ڣ���t2��ʱ���Ȼ��غ�����������ʵ��ܽ����ȣ��۽��½ᾧ���ܱ��ͣ�2��5��
����������1�����������У�ˮ�����ˣ��ܼ����������٣����ʵ��������䣻������䣻
��2���ٴ������ķ�Ӧ���Ȼ�þ���������Ʒ�Ӧ����������þ�������Ȼ��ƣ����ڸ��ֽⷴӦ��������ֽ⣻
��3����ͨ�������ܽ�����ߣ����Կ�����t1��ʱ���Ȼ��ص��ܽ�ȴ�������ص��ܽ�ȣ�����KCl������Һ������������������KNO3������Һ����������������
������ڣ�
��t2��ʱ���Ȼ��غ�����������ʵ��ܽ�������ཻ��˵�����¶��¶��ߵ��ܽ����ȣ��ʴ𰸣�t2��ʱ���Ȼ��غ�����������ʵ��ܽ����ȣ�
��KNO3���ܽ���ܶȱ仯Ӱ��ϴ�KCl���ܽ�����¶�Ӱ���С��������KNO3�л�������KCl�������ý��½ᾧ�ķ����ᴿKNO3��������½ᾧ��
��20��ʱ��KNO3���ܽ��Ϊ31.6g��80��ʱ��KNO3���ܽ��Ϊ169g����20��ʱ����ʢ��200gˮ���ձ��м���80gKNO3���ܽ�������Ϊ63.2g�����Եõ����¶�ʱKNO3�ı�����Һ����ʹ�ձ������ʻ���������80�棬�ڸ��¶��£�����ȫ���ܽ⣬�������������Һ���������ܼ�������֮��Ϊ80g��200g=2��5��������ͣ�2��5��

 ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д� �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
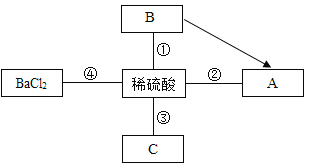
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�����Ŀ������ѡ�õij����Լ���ʵ���������ȷ���ǣ�������Ϊ���ʣ��� ��
���� | �����Լ� | �������� |
A�� CO2��HCl�� | ����������Һ | ����ͨ��ʢ������������Һ��ϴ��ƿ |
B�� NaCl��Na2CO3�� | ����������Һ | ������������������Һ�����ˡ��������ᾧ |
C�� MnO2��NaCl�� | ˮ | ��������ˮ�ܽ⡢���ˡ�ϴ�ӡ����� |
D�� Cu��CuO�� | ���� | ͨ���������������� |
A��A B��B C��C D��D