题目内容
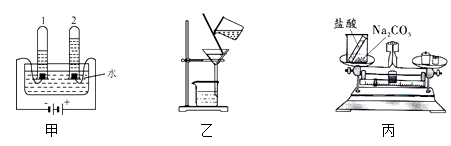
【题目】某化学兴趣小组的同学们欲测定一定量的某种石灰石样品中碳酸钙的质量,进行了如下实验: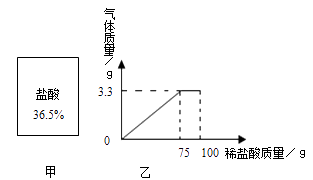
(1)配制100g溶质质量分数为7.3%的稀盐酸,需图甲所示盐酸的质量为g。
(2)将(1)中配制好的稀盐酸加人盛有石灰石样品的烧杯中,产生气体的质量与加入稀盐酸的质量关系如图乙所示(假设石灰石样品中的杂质不与稀盐酸反应)。计算:该石灰石样品中碳酸钙的质量。
【答案】
(1)20
(2)解:设 参加反应的碳酸钙的质量为x
CaCO3+ | 2HCl═ | CaCl2+H2O+ | CO2↑ |
100 | 44 | ||
x | 3.3g |
列比例式得:100:X=44:3.3克 解得x = 7.5g
CaCO3+ | 2HCl═ | CaCl2+H2O+ | CO2↑ |
100 | 73 | ||
x | 75g×7.3% |
列比例式得:100:X=73:(75g×7.3%)x = 7.5g
答:该石灰石样品中碳酸钙的质量为7.5g
【解析】(1)用这瓶浓盐酸来配制100g溶质质量分数为7.3%的稀盐酸,需量取这种浓盐酸的质量是=(100克×7.3%)/36.5%=20g;(1)根据稀释前后溶液中溶质的质量不变解答
(2)由图像可知二氧化碳的质量是3.3g,利用二氧化碳的质量结合方程式即可解答

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案
相关题目