题目内容
【题目】某化合物R3.2g在空气中充分燃烧只生成8.8g二氧化碳和7.2g水,下列对化合物R的叙述中正确的是( )
A. R由碳、氢、氧三种元素组成 B. R中碳、氢、氧元素的质量比为2:6:1
C. R的化学式是CH4 D. R中碳、氢原子个数比为3:1
【答案】C
【解析】
先根据质量守恒定律:反应前后元素的种类不变,确定:该物质中一定含有碳、氢两种元素,可能含有氧元素;再根据反应前后元素的质量相等,来确定氧元素是否含有;8.8g二氧化碳中碳元素的质量=8.8g×![]() ×100%=2.4g, 7.2g水中氢元素的质量=7.2g×
×100%=2.4g, 7.2g水中氢元素的质量=7.2g×![]() ×100%=0.8g, 2.4g+0.8g=3.2g与物质的质量相等,故一定不含氧元素;R中碳、氢原子个数比为:
×100%=0.8g, 2.4g+0.8g=3.2g与物质的质量相等,故一定不含氧元素;R中碳、氢原子个数比为:![]() =1:4,故R的化学式是CH4。故选C。
=1:4,故R的化学式是CH4。故选C。

练习册系列答案
相关题目
【题目】下图是制取二氧化碳并进行有关物质的性质实验的装置。请根据要求回答有关问题。
查阅资料可知:氢氧化钠可以吸收二氧化碳,反应的方程式为:CO2+2NaOH=Na2CO3+H2O
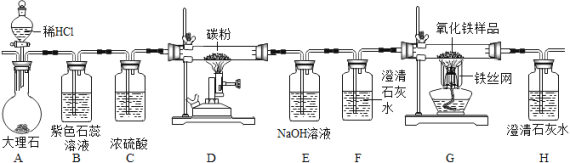
(1)写出下列装置中的化学方程式:装置A:______,装置G__________
(2)实验过程中装置B中的现象是_________装置F的作用是_______
(3)将A中的稀盐酸不断滴入大理石后,应先点燃_________(选填D或G处)的酒精灯。
(4)充分反应前后G装置的质量分别表示于右下表中,则样品中氧化铁的的质量为_____g
G | |
反应前(g) | 57.8 |
反应后(g) | 55.4 |
(5)该装置有一处明显的不足,请你给出改进的具体措施_________